
科目: 来源: 题型:
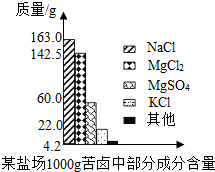 海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.下图是我市某盐场苦卤中部分成分含量柱形图.试计算:
海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.下图是我市某盐场苦卤中部分成分含量柱形图.试计算:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 (2007?南通)已知A、B、C三种固体含有同种金属元素,A难溶于水,B是一种氧化物,可作为干燥剂.D、E、F含有同种非金属元素,E是常见的固体单质,D、F通常状况下为气体.X由两种元素组成,其中E元素的质量分数为37.5%,与另一种元素原子个数比为2:1.它们的转化关系如下图(部分产物已略去).
(2007?南通)已知A、B、C三种固体含有同种金属元素,A难溶于水,B是一种氧化物,可作为干燥剂.D、E、F含有同种非金属元素,E是常见的固体单质,D、F通常状况下为气体.X由两种元素组成,其中E元素的质量分数为37.5%,与另一种元素原子个数比为2:1.它们的转化关系如下图(部分产物已略去).
查看答案和解析>>
科目: 来源: 题型:
|
族 周期 |
ⅠA | |||||||
| 1 |
1H 氢 |
ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 |
6C 碳 |
xN 氮 |
8O 氧 |
|||||
| 3 |
llNa 钠 |
12Mg 镁 |
15P 磷 |
16S 硫 |
17C1 氯 | |||
| 4 |
19K 钾 |
20Ca 钙 |
… | |||||
查看答案和解析>>
科目: 来源: 题型:
(2007?南通)下表是20℃时硫酸溶液和氨水的密度与其溶质的质量分数对照表.下列说法正确的是( )
|
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com