
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.如图是某盐场苦卤中部分成分含量柱形图.试计算:
海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.如图是某盐场苦卤中部分成分含量柱形图.试计算:查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| 0℃ | 20℃ | 40℃ | 60℃ | |
| NaHCO3 | 6.9 | 9.6 | 12.7 | 16.4 |
| NaCl | 35.7 | 35.8 | 36.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
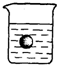 25、有一盛有100mL49%硫酸溶液的烧杯,同时有一表面光滑的塑料小球悬浮于溶液中央(如图所示).现向该溶液中缓慢注入20%的Ba(OH)2溶液至恰好完全反应,在此实验过程中:
25、有一盛有100mL49%硫酸溶液的烧杯,同时有一表面光滑的塑料小球悬浮于溶液中央(如图所示).现向该溶液中缓慢注入20%的Ba(OH)2溶液至恰好完全反应,在此实验过程中:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com