
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 (2012?塘沽区一模)如图是实验室里的一瓶硫酸溶液,请根据下面的内容进行计算:
(2012?塘沽区一模)如图是实验室里的一瓶硫酸溶液,请根据下面的内容进行计算:查看答案和解析>>
科目: 来源: 题型:阅读理解
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放入试管中加水溶解,滴入适量的澄清石灰水 | 产生白色沉淀 | 猜想一正确 |
| 取上层清液放入另一只试管中,滴加酚酞溶液 | 溶液变红 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放入试管中加水溶解,滴入足量的 氯化钙溶液 氯化钙溶液 . |
产生白色沉淀 | 猜想一正确 |
| 取上层清液放入另一只试管中,滴加酚酞溶液 | 溶液变红 |

查看答案和解析>>
科目: 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
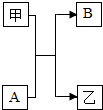 (2012?塘沽区一模)(1)在分开盛放的A、B两种溶液中,共含有Na+、H+、Ag+、Ba2+、NO3-、Cl-、CO32-七种离子,已知A溶液中含有三种阳离子和一种阴离子,则B溶液中所含的离子是
(2012?塘沽区一模)(1)在分开盛放的A、B两种溶液中,共含有Na+、H+、Ag+、Ba2+、NO3-、Cl-、CO32-七种离子,已知A溶液中含有三种阳离子和一种阴离子,则B溶液中所含的离子是查看答案和解析>>
科目: 来源: 题型:
 (2012?塘沽区一模)请回忆“溶液”单元的知识,回答下列问题:
(2012?塘沽区一模)请回忆“溶液”单元的知识,回答下列问题:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
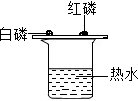 (2012?塘沽区一模)燃料的燃烧在人类社会的发展中起着相当重要的作用.
(2012?塘沽区一模)燃料的燃烧在人类社会的发展中起着相当重要的作用.
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com