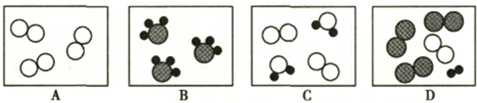
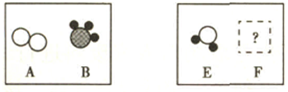
在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究.如图实验装置和选用药品,现分别以A、B、C、D表示如图所示:

A、B、C三个实验分别由甲、乙、丙三个组的同学来完成,D实验由丁组同学对镁条燃烧前后分别进行称量,他们都进行了规范的操作、准确的称量和细致的观察.
(1)A实验:白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡.结论是:质量不守恒.待锥形瓶冷却后,重新放到托盘天平上称量,天平平衡.结论是:质量守恒.你认为结论正确的是
后一种
后一种
(填“前一种”或“后一种”),而导致另一种结论错误的原因是
白磷燃烧放出的热量使气体受热膨胀,小气球胀大产生浮力,使得天平不平衡
白磷燃烧放出的热量使气体受热膨胀,小气球胀大产生浮力,使得天平不平衡
.整个过程中小气球的变化是:
白磷燃烧时,小气球膨胀,冷却后,小气球缩小,到最后被吸瘪
白磷燃烧时,小气球膨胀,冷却后,小气球缩小,到最后被吸瘪
.
(2)丙组同学认为C实验说明了质量守恒.请你从原子的角度说明为什么?
因为反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变
因为反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变
;乙、丁两组同学得到的错误结论是“实验B、D均说明质量不守恒”.老师指导同学们分析了B、D两个实验反应前后天平不平衡的原因.你认为B实验天平不平衡的原因是
反应后生成的CO2逸出,使得天平不平衡
反应后生成的CO2逸出,使得天平不平衡
;D镁条燃烧前后,质量不相等的原因是
镁条燃烧结合了空气中的氧气,使得前后质量不相等.
镁条燃烧结合了空气中的氧气,使得前后质量不相等.
.

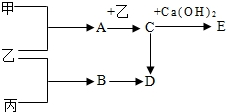

 三种小球分别代表氢原子、氧原子和氮原子.
三种小球分别代表氢原子、氧原子和氮原子.