(2013?太原)化学小组同学为鉴定某工厂排出的无色污水成分,他们查阅该工厂的有关资料后,推测出污水中可能含有HCl、Na
2SO
4、Na
2CO
3中的一种或几种物质,同学们取污水进行了如下探究:(已知Na
2SO
4溶液呈中性)
(1)测污水的pH:取一张pH试纸,放在玻璃片上
用玻璃棒蘸取污水样品,滴在pH试纸上,与标准比色卡比较
用玻璃棒蘸取污水样品,滴在pH试纸上,与标准比色卡比较
,读数为Ph=2,由此可知:污水中一定有
HCl
HCl
,可能有Na
2SO
4.
(2)检验Na
2SO
4是否存在:甲同学在一支试管中取少量污水,向试管中滴加少量的
BaCl2
BaCl2
溶液,振荡,产生了白色沉淀,反应的化学方程式为
Na2SO4+BaCl2═BaSO4↓+2NaCl
Na2SO4+BaCl2═BaSO4↓+2NaCl
(合理即可),证明污水中有Na2SO4存在.乙同学用物理方法也得到了同样的结论,他的实验操作及现象是
在试管中取少量污水样品蒸干,有白色固体析出
在试管中取少量污水样品蒸干,有白色固体析出
.
通过探究,同学们确定了污水的成分.
为使排放的污水中不含有酸或碱,可向污水中加过量的
石灰石(或铁屑)
石灰石(或铁屑)
(合理即可).

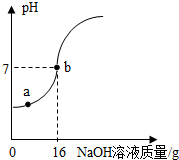 (2013?太原)实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数.现取10g稀硫酸样品,将5%的NaOH溶液逐滴加到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试回答:
(2013?太原)实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数.现取10g稀硫酸样品,将5%的NaOH溶液逐滴加到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试回答: