
在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.
(提出问题)结块后的固体成分是什么?
(猜想与假设)猜想一:固体为碳酸钠 猜想二:固体为碳酸钠和氢氧化钠.
用化学方程式表示固体中有碳酸钠的原因
CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
.
(查阅资料) Na
2CO
3溶液pH>7,BaCl
2溶液pH=7,Na
2CO
3+BaCl
2=BaCO
3↓+2NaCl
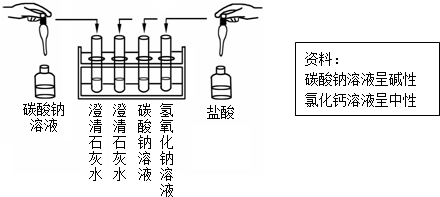
(进行实验)从瓶中取出一定量的固体,加入足量水溶解,再将溶液分三等份分别装入A、B、C三支试管,进行如下实验.
同学们根据实验现象,认为结块固体中有碳酸钠和氢氧化钠.
(实验分析)
(1)根据同学们的实验结论,三支试管中观察到的实验现象分别是
A中溶液变红
A中溶液变红
、
B中有气泡产生
B中有气泡产生
、
C中溶液变浑浊
C中溶液变浑浊
;
B试管中现象产生的原因是(用化学方程式表示)
Na2CO3+2HCl═2NaCl+H2O+CO2↑
Na2CO3+2HCl═2NaCl+H2O+CO2↑
.
(2)同学们得出的结论是不正确的,原因是
碳酸钠溶液呈碱性,A中滴加无色酚酞溶液后变红,不能证明原固体有氢氧化钠
碳酸钠溶液呈碱性,A中滴加无色酚酞溶液后变红,不能证明原固体有氢氧化钠
.
(实验设计)为进一步确定固体的成分,请写出你设计的实验方案
取少量结块固体于试管(或烧杯)中,加水使其完全溶解,再向其中加入过量的氯化钡溶液,静置后,向上层清液(或过滤后向滤液)中滴加几滴无色酚酞溶液,若溶液变红,则结块固体中有氢氧化钠,否则,无氢氧化钠
取少量结块固体于试管(或烧杯)中,加水使其完全溶解,再向其中加入过量的氯化钡溶液,静置后,向上层清液(或过滤后向滤液)中滴加几滴无色酚酞溶液,若溶液变红,则结块固体中有氢氧化钠,否则,无氢氧化钠
.
(实验反思)
(1)试剂瓶中的固体结块的原因可能是
氢氧化钠吸水潮解
氢氧化钠吸水潮解
.
(2)在溶解固体时放出了一定的热量,依据此现象有同学认为该固体中一定有氢氧化钠,为验证该同学的结论是否正确,还应该进行的实验是
取碳酸钠固体将其溶解,观察是否有放热现象
取碳酸钠固体将其溶解,观察是否有放热现象
.

 在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.
在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.

 (2013?平谷区模拟)下列数据是氯化钠和氯化铵固体在不同温度时的溶解度.
(2013?平谷区模拟)下列数据是氯化钠和氯化铵固体在不同温度时的溶解度.