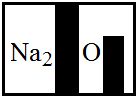
(2013?白云区一模)某校化学兴趣小组在实验室发现了一瓶标签受到腐蚀的溶液(如图).他们对该溶液是什么产生了兴趣.开始探究这瓶溶液究竟是什么?经过询问实验老师得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的一种,为了确定该药品,他们首先根据标签上残留的信息进行了分析:
(1)小明认为既然组成中含有氧元素,该溶液一定不是
氯化钠
氯化钠
溶液.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据
碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1
碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1
.
(3)为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验:取少量样品于试管中,慢慢滴加BaCl
2溶液,发现有白色沉淀产生.为了进一步检验该沉淀究竟是哪种物质,他们又向沉淀中滴加稀盐酸,结果发现沉淀溶解并产生大量气泡.由此他们得到的结论是:这瓶溶液是
碳酸钠溶液
碳酸钠溶液
,生成沉淀的反应化学方程式为
Na2CO3+BaCl2=BaCO3↓+2NaCl
Na2CO3+BaCl2=BaCO3↓+2NaCl
.
(4)在总结反思本次探究活动时,小强认为这个检测实验还可简化,照样可达到目的.小强的做法是
向溶液中加入盐酸
向溶液中加入盐酸
.其理由
碳酸钠能与盐酸反应生成二氧化碳气体,而硫酸钠不能与盐酸反应
碳酸钠能与盐酸反应生成二氧化碳气体,而硫酸钠不能与盐酸反应
.



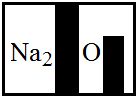 (2013?白云区一模)某校化学兴趣小组在实验室发现了一瓶标签受到腐蚀的溶液(如图).他们对该溶液是什么产生了兴趣.开始探究这瓶溶液究竟是什么?经过询问实验老师得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的一种,为了确定该药品,他们首先根据标签上残留的信息进行了分析:
(2013?白云区一模)某校化学兴趣小组在实验室发现了一瓶标签受到腐蚀的溶液(如图).他们对该溶液是什么产生了兴趣.开始探究这瓶溶液究竟是什么?经过询问实验老师得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的一种,为了确定该药品,他们首先根据标签上残留的信息进行了分析:
 (2013?白云区一模)下表是NaCl和KNO3在不同温度时的溶解度,请根据相关信息回答下列问题.
(2013?白云区一模)下表是NaCl和KNO3在不同温度时的溶解度,请根据相关信息回答下列问题.