某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
(1)如图1所示装置和药品进行实验,实验中可观察到的现象是
红磷剧烈燃烧产生大量白烟,同时释放出大量的热,待装置冷却到室温打开止水夹,水倒流至瓶中约1/5 处.
红磷剧烈燃烧产生大量白烟,同时释放出大量的热,待装置冷却到室温打开止水夹,水倒流至瓶中约1/5 处.
.该反应的文字表达式为
.
(2)甲同学认为可用木炭代替红磷测定空气中氧气的含量,乙同学 认为不可以,其原因是:
木炭燃烧产生CO2是气体,瓶内压强不变,水不会倒流
木炭燃烧产生CO2是气体,瓶内压强不变,水不会倒流
.乙同学用图1实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其原因可能是(答出一种即可):
红磷不足(未冷却到室温读数,装置漏气)
红磷不足(未冷却到室温读数,装置漏气)
.
(3)丙同学用镁条代替红磷来测定空气中氧气的含量.结果却发现倒吸的水量远远超过集气瓶的1/5.小组内同学帮她仔细检查,发现装置的气密性及操作步骤均无问题.你认为造成此现象的原因可能是
镁也和空气中的其它气体成分(如氮气)发生了化学反应
镁也和空气中的其它气体成分(如氮气)发生了化学反应
.
(4)小组内同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是:
本身是固体,只能够和空气中氧气或者氮气等单一物质反应,生成物是固体(若不是固体,可选择可以吸收该气体的液体来代替水)
本身是固体,只能够和空气中氧气或者氮气等单一物质反应,生成物是固体(若不是固体,可选择可以吸收该气体的液体来代替水)
.
(5)小组内同学还对该实验进行了如下改进.(已知试管容积为 45mL)
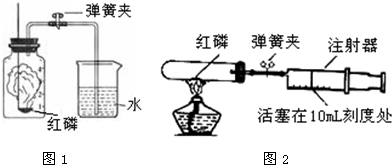
实验的操作步骤如下:①点燃酒精灯.②撤去酒精灯,待试管冷却后松开弹簧夹.③将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图2中所示的连接方式固定好,再将弹簧夹紧橡皮管.④读取注射器活塞的数据.
你认为正确的实验操作顺序是
③①②④
③①②④
(填序号).注射器活塞将从10mL刻度处慢慢前移到约为
1
1
mL刻度处才停止.
(6)此实验还可推知反应后剩余气体的两点性质是
不能燃烧,也不能支持燃烧,(不易溶于水)
不能燃烧,也不能支持燃烧,(不易溶于水)
.


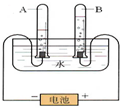 甲同学在探究水的组成实验时(装置如图所示).通电一段时间后,试管A、B中所收集的气体体积比为
甲同学在探究水的组成实验时(装置如图所示).通电一段时间后,试管A、B中所收集的气体体积比为