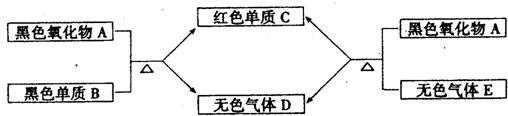
(2010?溧阳市模拟)请你参与下列探究.
【问题情景】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同
时,有较多的气泡放出.这一现象激发起同学们的探究欲望,生成的是什么气体呢?
【提出猜想】从物质组成元素的角度分析,放出的气体可能是S0
2、0
2、H
2.
【查阅资料】S0
2易溶于水,它能与NaOH溶液反应,生成Na
2S0
3.
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是0
2,则检验方法是
用带火星的木条伸入收集的气体中若复燃说明是氧气
用带火星的木条伸入收集的气体中若复燃说明是氧气
.
(2)乙同学认为是S0
2,则只需将放出的气体通人盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量.写出S0
2与NaOH反应的化学方程式:
S02+2NaOH=Na2S03+H2O
S02+2NaOH=Na2S03+H2O
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.
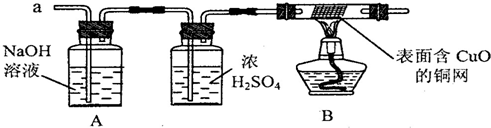
如果放出的是0
2和H
2的混合物,你认为方案中的安全隐患是
在B中加热可能会爆炸
在B中加热可能会爆炸
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指
堵住试管口迅速移近酒精灯
堵住试管口迅速移近酒精灯
,若不发出
尖锐的爆鸣声
尖锐的爆鸣声
,方可采用上面的装置进行实验.
【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通人,过一会儿点燃B处酒精灯;一段时间后,发现表面含Cu0的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量不变,确认反应中没有S0
2生成.
结论:
(1)铁粉与硫酸铜溶液反应时,产生的气体是
H2
H2
.
(2)写出H:和氧化铜在加热条件下反应的化学方程式:
【思维拓展】
(1)由上述实验可以推出,硫酸铜溶液显
酸
酸
(选填“酸”或“碱”)性.
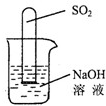
(2)有一同学提出:不通过称量,也能说明有无S0
2生成.他设计了右图所示的装置进行实验,发现试管内液面上升,就得出S0
2与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是
空气中的二氧化硫也能和氢氧化钠反应使试管中的气压减小,试管中液面上升
空气中的二氧化硫也能和氢氧化钠反应使试管中的气压减小,试管中液面上升
.