
科目: 来源: 题型:
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 1.砂纸 |
| 打磨 |
| 2.除锈液浸泡 |
| 煮沸5-10min |
| 3.除锈液浸泡 |
| 60-70℃ |
| 4.发蓝液浸泡 |
| 煮沸20min |
| 5.重铬酸钾溶液浸泡 |
| 煮沸约10分钟 |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
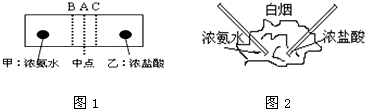
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com