实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物,极易与空气中水蒸气和CO
2反应而变质.同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究.
(1)【猜想】
猜想Ⅰ:没有变质,“碱石灰”中只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO
3和 Na
2CO
3(2)【实验】如图所示:
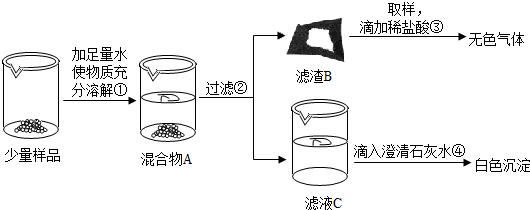
实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热.
(3)【判断】
a.若Ca(OH)
2、CaCO
3和Na
2CO
3溶于水无明显的温度变化,则猜想Ⅱ
不成立
不成立
;(填“成立”或“不成立”)
b.操作③发生反应的化学方程式为
CaCO3+2HCl═CaCl2+CO2↑+H2O
CaCO3+2HCl═CaCl2+CO2↑+H2O
;
由操作④的现象判断:滤液C中的溶质一定含有
Na2CO3
Na2CO3
(写化学式);
由此判断猜想Ⅰ
不成立
不成立
(填“成立”或“不成立”)
c.综合a和b的结论,判断该样品变质情况为
部分变质
部分变质
(填“全部变质”或“部分变质”)
下列对样品成分的分析正确的是
②③
②③
(填序号).
①样品中一定含NaOH
②样品中一定含Na
2CO
3③样品中含NaOH、CaO中的一种或两种
【拓展】由上述实验说明,实验室中“碱石灰”应
密封
密封
保存;操作②中玻璃棒的作用是
引流
引流
.



 橄榄油 B.
橄榄油 B. 蔬菜 C.
蔬菜 C. 米饭
米饭