(2013?武汉)某化学兴趣小组完成了如图所示的化学实验(装置气密性良好),证明了二氧化碳的组成.
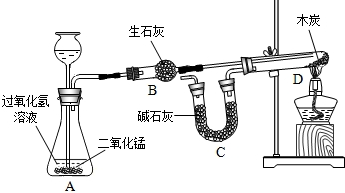
探究过程如下:I.称量装有干燥块状木炭的试管D,质量为50.7g,装有碱石灰的干燥管质量为112.3g,连接A、B、D装置;
II.从从长颈漏斗中加入3%的过氧化氢溶液,连接C装置,点燃酒精灯;
III.待D中发生反应,熄灭酒精灯,冷却;
IV.称量试管D及剩余固体质量为50.1g,装置C的质量为114.5g.
已知:碱石灰主要成分是氧化钙和氢氧化钠,木炭中的杂质不参加反应,B、C中所装药品是足量的能够完全吸收相关物质.请回答下列问题:
(1)装置A中发生反应的化学方程式为
,该反应属于
分解
分解
反应;
(2)酒精灯的作用是
点燃木炭
点燃木炭
;
(3)为减少误差,步骤III冷却过程中需要注意的问题是
继续通氧气
继续通氧气
;
(4)根据实验数据计算参加反应的氧气质量为
(114.5g-112.3g)-(50.7g-50.1g)=1.6g
(114.5g-112.3g)-(50.7g-50.1g)=1.6g
(列示并计算计算结果);从而计算出二氧化碳中碳、氧元素质量之比.


 (2013?武汉)如图是甲、乙、丙三种物质的溶解度曲线.
(2013?武汉)如图是甲、乙、丙三种物质的溶解度曲线.