
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| 实验步骤 | 预测现象 | 相应的结论 |
| (1)用试管分别取四种溶液,向其中分别滴加酚酞试液 | 有一支试管中的溶液由无色变为红色 有一支试管中的溶液由无色变为红色 |
该试管中的物质是NaOH溶液 |
| (2) 2)将滴有酚酞的NaOH溶液分别滴入盛有其它三种无色溶液的试管中 2)将滴有酚酞的NaOH溶液分别滴入盛有其它三种无色溶液的试管中 |
有一支试管中产生白色沉淀 | 该试管中的原物质是MgSO4溶液 该试管中的原物质是MgSO4溶液 |
有一支试管中滴有酚酞的NaOH溶液褪色 有一支试管中滴有酚酞的NaOH溶液褪色 |
该试管中的原物质是HNO3溶液 | |
| 有一支试管中没有明显现象 | 该试管中的原物质是NaCl溶液 |
查看答案和解析>>
科目: 来源: 题型:
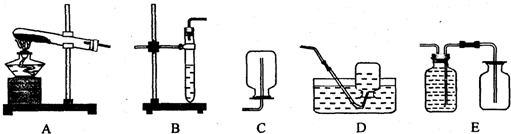
| ||
| ||
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com