
科目: 来源: 题型:
 (2005?扬州)研究性学习课题:实验室中久置的NaOH的变质程度
(2005?扬州)研究性学习课题:实验室中久置的NaOH的变质程度| Na2CO3的质量/g | 5.3g 5.3g |
| 变质NaOH的质量/g | 4.0g 4.0g |
| NaOH的变质程度(用质量分数表示) | 66.7% 66.7% |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 12 |
| 222 |
| 12 |
| 222 |
| 步 骤 | 现 象 | 结论(化学方程式) | ||||||||
取黑色粉末放于试管中加强热,并将生成气体通入澄清石灰水中 取黑色粉末放于试管中加强热,并将生成气体通入澄清石灰水中 |
粉末由黑色变成红色,石灰水变浑浊 粉末由黑色变成红色,石灰水变浑浊 |
2CuO+C
2CuO+C
|
查看答案和解析>>
科目: 来源: 题型:阅读理解
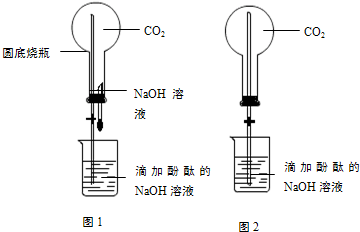
查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com