
科目: 来源: 题型:阅读理解
| 实验内容和步骤 | A | B | C | 结论或解释 | |
| 碳酸氢铵 | 碱式碳酸铜 | 碳酸钙 | |||
| 1.外观对比,观察其颜色、状态、气味. | 白色粉末 氨臭味 |
① 绿色粉末,无气味 绿色粉末,无气味 |
白色粉末 无气味 |
碳酸氢铵不稳定,易分解 | |
| 2.与水作用,各取固体试剂少许,分别按序号连续操作. | (1)加水少许,振荡后静置 | 无色澄清溶液 | 上层澄清,固体不溶解 | 液体浑浊 | 铵盐易溶于水 |
| (2)取清液测其pH | 8 | 7 | 8 | 盐又可分为酸式盐、碱式盐和正盐,从(2)实验的结果可知盐的酸碱性与其分类② 没有 没有 关(填“有”或“没有”) | |
| (3)滴加酚酞试液,振荡 | 无色 | 无色 | ③ 粉红 粉红 |
A、B、C加热前后的对比说明 ④ 温度 温度 对反应有影响 | |
| (4)将试管置于烧杯内热水水浴 | 略有粉红色 | 略有粉红色 | 粉红色略有加深 | ||
| 3.与酸或碱作用,各取固体试剂少许2份,分别滴加右侧试剂. | (1)体积比浓度1:2盐酸 | 快速冒出气泡,形成无色溶液 | ⑤ 快速冒出气泡,形成蓝色溶液 快速冒出气泡,形成蓝色溶液 |
快速冒出气泡,形成无色溶液 | 将C与石灰石和盐酸的反应对比可以看出⑥ 反应物的颗粒大小影响反应的剧烈程度 反应物的颗粒大小影响反应的剧烈程度 |
| (2)10%氢氧化钠溶液 | 无明显现象或略有氨臭味,形成无色溶液 | ⑦ 生成蓝色溶液 生成蓝色溶液 |
无明显现象 | B中反应说明 ⑧ 碱式盐可与碱反应 碱式盐可与碱反应 | |
查看答案和解析>>
科目: 来源: 题型:
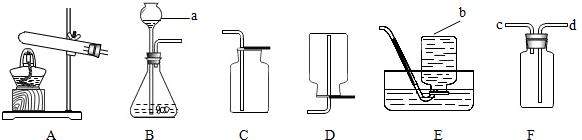
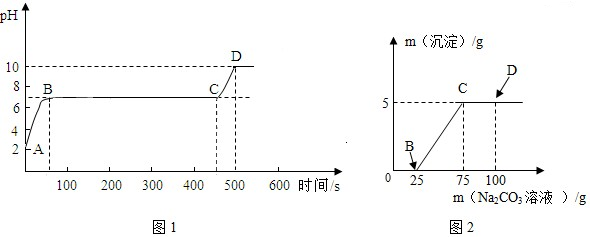
查看答案和解析>>
科目: 来源: 题型:
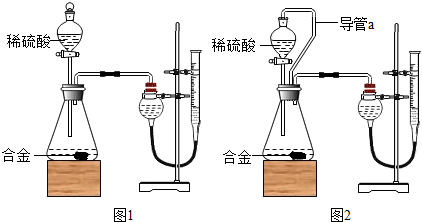
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A | B | C | |
| 反应信息 | H2和O2反应 | 电解水 | 水与Na反应生成NaOH和H2 |
| 反应类型 | 化合反应 | 分解反应 | 置换反应 |
查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
| ||
| 叶绿素 |
| ||
| 叶绿素 |
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
| 序号 | (1) | (2) | (3) | (4) | (5) |
| 名称 | 氮气 | 氢氧化亚铁 氢氧化亚铁 |
酒精 | 碳酸氢铵 | 亚硝酸钠 |
| 化学式 | N2 N2 |
Fe(OH)2 | C2H5OH | NH4HCO3 | NaNO2 NaNO2 |
| 类别 | 单质 | 碱 碱 |
有机物 有机物 |
酸式盐 酸式盐 |
正盐 |
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如下表所示.下列未知数据计算正确的是( )
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com