小明对实验室制取二氧化碳的实验进行了相关探究.
(1)请你和小明一起进行实验室制取二氧化碳药品选择的探究.
小明对三组药品进行了研究,实验记录如下:
| 组别 |
药品 |
实验现象 |
| ① |
块状石灰石和稀盐酸 |
产生气泡速率适中 |
| ② |
块状石灰石和稀硫酸 |
产生气泡速率缓慢并逐渐停止 |
| ③ |
碳酸钠粉末和稀盐酸 |
产生气泡速率很快 |
从制取和收集的角度分析,一般选择第①组药品,所发生反应的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;不选择第③组药品的原因是
反应速度太快
反应速度太快
.
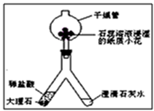
(2)利用如图所示装置进行二氧化碳的制备和性质实验.实验进行一段时间后,“人”字管右端可以观察到的现象是
澄清的石灰水变浑浊
澄清的石灰水变浑浊
,发生反应的化学方程式为
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
,被石蕊溶液浸湿的纸质小花的颜色变化为
红色
红色
,若将
燃着
燃着
的木条从干燥管的上管口伸入管内,可以看到
熄灭
熄灭
,说明二氧化碳具有
既不燃烧也不支持燃烧
既不燃烧也不支持燃烧
的性质.
| 吸收液的种类/100mL |
被吸收的CO2体积/mL |
| 蒸馏水 |
82.9 |
| 饱和NaCl溶液 |
58.6 |
| 饱和Na2SO4溶液 |
56 |
| 饱和NaHCO3溶液 |
120 |
(3)利用向上排空气法往往不易得到纯净的CO
2.通过查阅资料可知:25℃时,CO
2在水和部分盐溶液中的溶解情况如下:
有人根据CO
2在水中能跟跟Na
2CO
3反应生成NaHCO
3,而NaHCO
3不跟CO
2反应的原理,提出用排饱和而NaHCO
3溶液的方法收集纯净的CO
2,可能行吗?
不能
不能
,原因是:
饱和碳酸氢钠吸收的二氧化碳的能力较强
饱和碳酸氢钠吸收的二氧化碳的能力较强
;你认为收集纯净CO
2较科学的方法是
用排饱和硫酸钠溶液的方法
用排饱和硫酸钠溶液的方法
.

 小明对实验室制取二氧化碳的实验进行了相关探究.
小明对实验室制取二氧化碳的实验进行了相关探究.