
科目: 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 分别取少量样品于试管中,向试管中加入 紫色石蕊试液 紫色石蕊试液 ,振荡,观察现象. |
能使紫色石蕊试液变红的 能使紫色石蕊试液蓝色的 能使紫色石蕊试液变红的 能使紫色石蕊试液蓝色的 |
是硫酸溶液 是氢氧化钠溶液 是硫酸溶液 是氢氧化钠溶液 |
查看答案和解析>>
科目: 来源: 题型:
| 操作 | 装置 | 现象 |
| 1、取一小块铜丝网,卷成筒形,固定在铜丝上. | 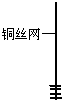 |
|
| 2、分别向①和②中注入15mL、30%的H2O2,并放入盛有热水的③中. | 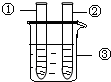 |
约1min后可观察到① 和②中都有少量气泡产生 |
| 3、把铜丝插入①中. | 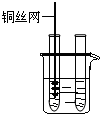 |
①中有大量气泡产生,约5min后不再有气泡产生;此时②中 仍然有少量气泡产生 |
查看答案和解析>>
科目: 来源: 题型:

| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
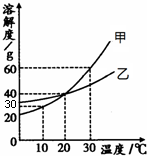
查看答案和解析>>
科目: 来源: 题型:
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g?cm-3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com