同学们在用某硫酸溶液处理金属废料(主要是生铁)时,观察到溶液发烫并闻到刺激性气味,这种反常现象引起同学们的思考.从元素组成的角度分析,他们猜测气体可能是SO
2、CO、CO
2、H
2中的一种或几种.

(1)甲同学认为废气中一定有SO
2,原因是
上述气体中只有SO2有刺激性气味
上述气体中只有SO2有刺激性气味
.
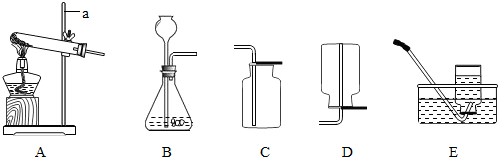
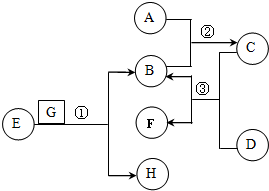
(2)为了确定该气体的成分,同学们设计了一套合理的实验装置,如下图所示(铁架台已略去).请你从下列试剂中选择药品并结合实验装置完成实验.
药品:澄清石灰水,酸性高锰酸钾溶液,无水硫酸铜(遇水变蓝),碱石灰(吸收水和CO
2). (药品可重复选用,每一步均反应充分)

(Ⅰ)B中盛放的试剂是
澄清石灰水
澄清石灰水
,A、B装置不能互换,原因是:
SO2也能使澄清石灰水变浑浊,无法判断是否含有CO2
SO2也能使澄清石灰水变浑浊,无法判断是否含有CO2
.
(Ⅱ)若观察到
D中的固体由红变黑,E中无明显变化,F中澄清石灰水变浑浊;
D中的固体由红变黑,E中无明显变化,F中澄清石灰水变浑浊;
现象,证明原气体中有CO无H
2.写出D中反应的化学方程式
.
(Ⅲ)D中反应前有样品10g(样品中可能混有铁),完全反应后剩余固体7.6g,则原样品的成分为:
氧化铁:8g 铁:2g;
氧化铁:8g 铁:2g;
.(写出物质及其对应的质量)