
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ||
| 催化剂 |
| ||
| 催化剂 |
查看答案和解析>>
科目: 来源: 题型:
| 测定时刻 | 6:05 | 6:10 | 6:15 | 6:20 | 6:25 | 6:30 |
| PH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 |
查看答案和解析>>
科目: 来源: 题型:
| 化学符号 | Ag Ag |
nSO2 |
|
He He | ||
| 表示意义 | 一个银原子 | n个二氧化硫 n个二氧化硫 |
-3价的氮元素 -3价的氮元素 |
氦气 |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 实验步骤 | 实验现象 | 结论 |
| 先用PH试纸测定稀硫酸的PH,再逐渐滴加氢氧化钠溶液,并不断振荡,同时测定混合液的PH. | PH逐渐变大, 最后 PH≥7 |
稀硫酸与氢氧化钠溶液能发生反应 |
| 实 验 步 骤 | 实验现象 | 结论 |
| 稀硫酸与氢氧化钠溶液反应放热 |
| 实验步骤 | 实验现象 | 结论 |
| 取少量上述反应后的溶液于试管中,滴加硫酸铜溶液. | 若 生成蓝色沉淀 生成蓝色沉淀 |
氢氧化钠溶液过量 |
| 若没有明显现象 | 稀硫酸与氢氧化钠溶液恰好完全反应 |
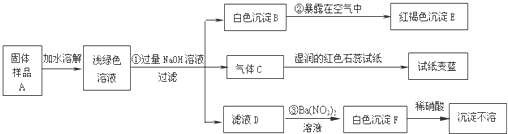
查看答案和解析>>
科目: 来源: 题型:

| ||
| ||

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com