(2006?仙桃)保护环境,爱护家园,从身边做起,是我们每个公民应尽的责任.学校实验室也会产生一些污染环境的有害气体和废液,请你一起参与环保行动.
(1)有害气体的认识和处理:
①实验室进行的下列实验,一定不会造成空气污染的是
C
C
(填编号).
A.实验室制取一氧化碳 B.硫在空气中燃烧
C.铁在氧气中燃烧 D.用灼烧的方法区分氯化钾和氯化铵固体
②为探究炼铁原理,设计了用CO还原赤铁矿(主要成分为Fe
2O
3)的实验,装置如下:
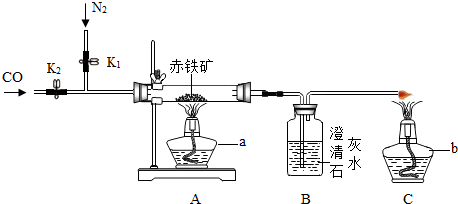
根据图示分析,酒精灯b的作用是
除去多余的CO,防止污染空气
除去多余的CO,防止污染空气
.实验结束后,应先熄灭的酒精灯是
a
a
(填“a”或“b”),此时,还应该改通氮气的目的是
用氮气排出装置内的CO,防止污染空气或隔绝空气冷却固体产物或防止倒吸等(任意答对其中一项给分)
用氮气排出装置内的CO,防止污染空气或隔绝空气冷却固体产物或防止倒吸等(任意答对其中一项给分)
.
(2)废液的处理:
某次实验结束后,废液缸中含有小纸屑、火柴棒、砂粒以及含FeCl
2、CuSO
4、H
2SO
4的废液,为防止污染环境,对其处理如下:
a.静置后将废液过滤,得滤液A;
b.向滤液A中加入稍过量的金属X,反应完毕后,过滤,得滤液B和滤渣Y.
c.向滤渣Y中加入适量的稀盐酸,过滤,得滤液C,并回收金属铜;
d.向滤液B中滴加适量的试剂Z至恰好反应,过滤,也得滤液C.
为了使回收后的滤液C是只含一种溶质的化学试剂,请回答下列问题:
①步骤b中加入的金属X为
铁(或Fe)
铁(或Fe)
.
②写出滤液B与试剂Z反应的化学方程式
BaCl2+FeSO4=BaSO4↓+FeCl2
BaCl2+FeSO4=BaSO4↓+FeCl2
.


