
科目: 来源: 题型:阅读理解
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入酚酞溶液 | 溶液变红 | 现象Ⅰ | 溶液变红 |
| 加入CuSO4溶液 | 产生气泡和蓝色沉淀 | 现象Ⅱ | 产生气泡和蓝色沉淀 |
| 加入CaCl2溶液 | 无明显变化 | 无明显变化 | 产生白色沉淀 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 |
澄清石灰水 变浑浊 |
澄清石灰水 无明显变化 |
澄清石灰水 无明显变化 |
| 实验操作 | 实验现象 | 实验结论 |
①取少量滤液于试管中,加入过量CaCl2溶液 ②过滤,向滤液中滴加CuSO4溶液 ①取少量滤液于试管中,加入过量CaCl2溶液 ②过滤,向滤液中滴加CuSO4溶液 |
①有白色沉淀生成 ②只产生蓝色沉淀,无气泡 ①有白色沉淀生成 ②只产生蓝色沉淀,无气泡 |
滤液中的溶质是Na2CO3和NaOH |
查看答案和解析>>
科目: 来源: 题型:
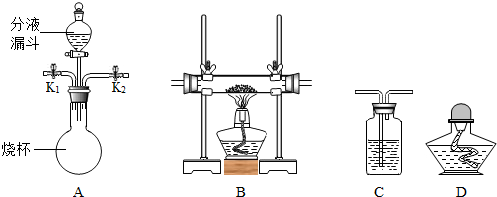
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:

| ||
| ||
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
 (2013?西城区一模)金属在生产生活中应用广泛.
(2013?西城区一模)金属在生产生活中应用广泛.
| ||
| 熔融 |
| ||
| 熔融 |
查看答案和解析>>
科目: 来源: 题型:
 (2013?西城区一模)食盐在生产和生活中具有广泛的用途.
(2013?西城区一模)食盐在生产和生活中具有广泛的用途.| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
| 溶液质量/g | 209 | 236 | 272 | 272 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com