
科目: 来源: 题型:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.836 | 5.672 | 8.508 |
| 生成气体的体积(标准状况)/L | 1.12 | 2.24 | 2.80 |
查看答案和解析>>
科目: 来源: 题型:
 自然界存在着一种白云石的矿石,其化学式是xCaCO3?yMgCO3.(其中x、y为最小正整数比).以它为原料,可制取耐火材料等.
自然界存在着一种白云石的矿石,其化学式是xCaCO3?yMgCO3.(其中x、y为最小正整数比).以它为原料,可制取耐火材料等.| 高温 |
| 高温 |
查看答案和解析>>
科目: 来源: 题型:
| ||
| A的用量 | B的用量 | A2B的质量 | |
| 甲 | 7.0 g | 1.0 g | 5.0 g |
| 乙 | 4.0 g | 4.0 g | 5.0 g |
| 丙 | a g | b g | 3.0 g |
查看答案和解析>>
科目: 来源: 题型:
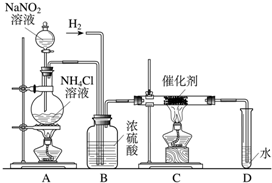
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
| 溶质 | CaSO4?2H2O | CaCO3 | BaSO4 |
| 溶解度 g/100gH2O | 0.201 | 0.0065 | 0.00017 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com