
科目: 来源: 题型:阅读理解
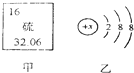
 如图所示是市某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,请认真阅读后解答下列问题.
如图所示是市某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,请认真阅读后解答下列问题.| 98 |
| 2 |
| 50×19.6% |
| y |
| 98 |
| 2 |
| 50×19.6% |
| y |
查看答案和解析>>
科目: 来源: 题型:
| 盐溶液 | NaCI | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品10.0g溶于50ml水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 产生白色沉淀 |
说明久置固体中,一定含有Na2CO3 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 |
说明久置固体中,还一定含有 NaOH NaOH |
查看答案和解析>>
科目: 来源: 题型:
| 名称 | 洗洁精 | 洁厕灵 | 炉具清洁剂 | 污渍爆炸盐 | 漂白粉 |
| 产品样式 |  |
 |
 |
 |
 |
| 有效成分或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过碳酸钠 | 消毒 |
查看答案和解析>>
科目: 来源: 题型:
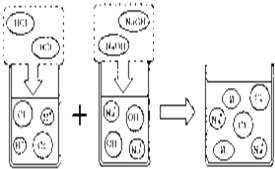
 (1)生活中处处有化学.请用下列物质的化学式填空:
(1)生活中处处有化学.请用下列物质的化学式填空:查看答案和解析>>
科目: 来源: 题型:
除去下列各物质中的少量杂质,所用方法不可行的是( )
|
查看答案和解析>>
科目: 来源: 题型:
下列整理的有关化学的知识内容完全正确的一组是( )
|
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1~2mL,滴入1~2滴无色酚酞试液,振荡 | 无色酚酞试液变 红色 红色 |
溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈 酸性 酸性 或中性 中性 |
查看答案和解析>>
科目: 来源: 题型:
| ||
| 400℃ |
| ||
| 400℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com