
科目: 来源: 题型:
用下列鉴别方法不能把待鉴别的物质区分开的是( )
|
查看答案和解析>>
科目: 来源: 题型:

| 反应的时间(min) | 3 | 6 | 9 | 12 | 15 |
| 电子天平读数(g) | 320.6 | 317.3 | 315.1 | M | 315.1 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
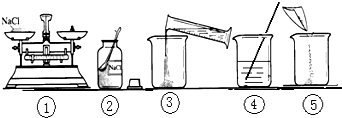
查看答案和解析>>
科目: 来源: 题型:
| 离子 | OH- | Cl- |
| ||
| H+ | 溶、挥 | 溶 | |||
| Na+ | 溶 | 溶 | 溶 | ||
| Ca2+ | 微 | 溶 | 微 | ||
| Ba2+ | 溶 | 溶 | 不 |
查看答案和解析>>
科目: 来源: 题型:
 甲、乙两种固体物质的溶解度曲线如图所示.
甲、乙两种固体物质的溶解度曲线如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com