
科目: 来源: 题型:
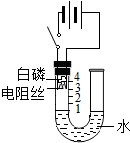 研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.其中U型管左侧容器壁上标有刻度,电阻丝通电后能发热,右侧玻璃管敞口.请根据图示实验回答下列问题:
研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.其中U型管左侧容器壁上标有刻度,电阻丝通电后能发热,右侧玻璃管敞口.请根据图示实验回答下列问题:
| ||
| ||
| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
科目: 来源: 题型:
| 操作 | 装置 | 现象 |
| 1、取一小块铜丝网,卷成筒形,固定在铜丝上. | 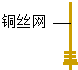 |
|
| 2、分别向①和②中注入15mL、30%的H2O,并放入盛有热水的③中. |  |
约1min后可观察到①和②中都有少量气泡产生 |
| 3、把铜丝插入①中. | 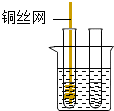 |
①中有大量气泡产生,约5min后不再有气泡产生;此时②中仍然有少量气泡产生 |
查看答案和解析>>
科目: 来源: 题型:
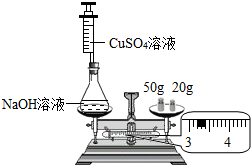 如图是某同学验证质量守恒定律实验的片段.
如图是某同学验证质量守恒定律实验的片段.查看答案和解析>>
科目: 来源: 题型:阅读理解
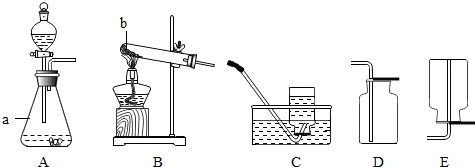
| ||
| △ |
| ||
| △ |
| 加热 |
| 加热 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
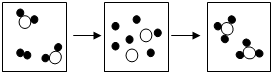 下面的示意图形象的表示某化学反应前后分子的变化,其中
下面的示意图形象的表示某化学反应前后分子的变化,其中  表示硫原子,
表示硫原子, 表示氧原子.
表示氧原子.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| -1 |
| Cl |
| -3 |
| N |
| -3 |
| N |
| ||
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com