
科目: 来源: 题型:
在一定条件下,向一密闭容器内加入A,B,C,D 4种物质各20g.充分反应后测定其质量,得到如下数据.
|
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 配料表:NaCl、KIO3、CaCO3 净含量:500g 成分表:NaCl≧88% 钙(以Ca计):(0.5~1.3)% 碘(以I计):(0.04~0.05)mg/g(1)KIO3的相对分子质量是 214 214 ;KIO3中碘元素的质量分数为59.3% 59.3% ;(2)一袋该食盐中KIO3的质量最多为 42.2 42.2 mg;(3)商标上的钙含量是指 钙元素 钙元素 (选填“单质钙”、“碳酸钙”、“钙元素”).
查看答案和解析>> 科目: 来源: 题型: 有一包从海水获得的粗盐,已经经过初步的提纯.某课外活动小组对它的成分进行探究,并将粗盐进一步提纯. 探究一 这包粗盐中还有什么杂质? (1)根据海水的成分和初步提纯的实验操作,估计该粗盐可能含有的杂质是CaCl2和MgCl2.实验证明,这包粗盐含有的杂质是CaCl2. 探究二 这包粗盐中NaCl的质量分数是多少? 按下面步骤继续实验: ①称取一定质量的样品; ②将样品加水溶解,制成粗盐溶液; ③向粗盐溶液中加过量的某种试剂,过滤; ④沉淀洗涤后小心烘干,得到纯净固体A; ⑤在所得的滤液中加入适量的一种试剂后,移入蒸发皿蒸发,得到纯净固体B; ⑥称量实验中得到的某种固体. 实验结束后,根据所称得的质量求出这包粗盐中NaCl的质量分数. (2)在②③⑤的步骤中,都使用到同一仪器(填名称) 玻璃棒 玻璃棒 ;在步骤③中的目的是引流防止液体溅出 引流防止液体溅出 .(3)步骤③中加入的试剂是(写化学式) Na2CO3 Na2CO3 ,步骤⑤中加入的试剂是稀盐酸 稀盐酸 ,目的是除去过量的碳酸钠 除去过量的碳酸钠 .(4)步骤⑥中,你认为需要称量的固体是固体A还是固体B(填A或B) A A ,你不选择称量另一种固体的理由是在反应的过程中,生成了新的氯化钠 在反应的过程中,生成了新的氯化钠 .查看答案和解析>> 科目: 来源: 题型: (1)人类从饮食中获取的营养素有糖类、油脂、无机盐、水、蛋白质、维生素等六大类.其中蛋白质属于有机高分子化合物,具有“四级结构”,具有生物活性,如果蛋白质与重金属离子,如Cu2+、Pb2+、Hg2+、Ba2+等接触,会因四级结构中某些级别的结构被破坏而失去生物活性,比如误服含Ba2+的物质会造成中毒.但病人在做“胃镜”检查时服用含有BaSO4的“钡餐”却不会造成中毒,原因是: 硫酸钡是不溶于水和酸的盐 硫酸钡是不溶于水和酸的盐 ;而误服BaCO3却会造成中毒,原因是(用化学方程式表示)BaCO3+2HCl═BaCl2+H2O+CO2↑ BaCO3+2HCl═BaCl2+H2O+CO2↑ .(2)下面框图中D广泛用于玻璃、造纸、纺织和洗涤剂的生产等,C在常温下为液体,K为非金属单质. 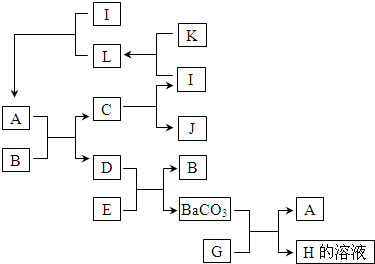 ①写出下列物质的化学式:B NaOH NaOH ,CH2O H2O ,EBa(OH)2 Ba(OH)2 ,LO2 O2 .②写出化学方程式:I+L→A 2CO+O2
2CO+O2 ;A+K→L
CO2+C
CO2+C .
③已知含Ba元素与Ca元素的化学性质相似,则BaCO3高温分解的化学反应方程式为: BaCO3
BaCO3 .
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |