小红同学发现班上“化学学习园地”的金属活动性顺序表(如图)中的Cu、Al、Fe三张卡片掉在地上,她将三张卡片依次贴回原来的位置.

(1)请在上述金属活动性顺序表的空格中填上小红同学所贴卡片上的元素符号.
(2)小红和化学兴趣小组的同学,根据所学的化学知识,用定影液(含AgNO
3)提取纯净金属银.他们设计了如下实验方案:
①a.向定影液中加入过量的锌粉,过滤;
b.向所得固体加入足量的稀硫酸,过滤,洗涤、晾干.
②a.向定影液中加入过量的铜粉,过滤;
b.向所得固体加入足量的稀硫酸,过滤,洗涤、晾干.
上述实验方案中能得到纯净金属银的是
①
①
(填“①”或“②”),其理由是
①得到的金属银含有的杂质锌可跟稀硫酸反应而除去,而方案②所得金属银中的杂质铜则不能
①得到的金属银含有的杂质锌可跟稀硫酸反应而除去,而方案②所得金属银中的杂质铜则不能
.
写出该方案中产生金属银的化学方程式:
Zn+2AgNO3=Zn(NO3)2+2Ag
Zn+2AgNO3=Zn(NO3)2+2Ag
.
(3)化学兴趣小组的其他同学对小红把掉下来的卡片贴的位置产生了怀疑.他们争论不休,各持己见.请你设计实验来证明小红的贴法是对的.实验所用材料和器具任选.写出实验步骤、现象及结论.
将三种金属放入三只试管中,然后加入稀盐酸,铝和铁的表面有气泡冒出,且铝表面冒出气泡的速度比铁块,铜不反应,可得出金属活动性铝>铁>铜
将三种金属放入三只试管中,然后加入稀盐酸,铝和铁的表面有气泡冒出,且铝表面冒出气泡的速度比铁块,铜不反应,可得出金属活动性铝>铁>铜
.
你还有别的设计方案吗?请你再设计一个实验.同样实验所用材料和器具任选.写出实验步骤、现象及结论.
将三种金属放入三只试管中,然后加入硫酸亚铁溶液,可发现铝的表面有铁析出,证明铝的活动性大于铁,铜的表面没有铁析出,证明铜的活动性小于铁,从而证明三种金属的活动性为铝>铁>铜;
将三种金属放入三只试管中,然后加入硫酸亚铁溶液,可发现铝的表面有铁析出,证明铝的活动性大于铁,铜的表面没有铁析出,证明铜的活动性小于铁,从而证明三种金属的活动性为铝>铁>铜;
.



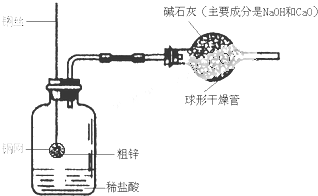 某同学设计了一套如下图所示的装置,并用该装置测定粗锌样品的含锌量.
某同学设计了一套如下图所示的装置,并用该装置测定粗锌样品的含锌量.