
科目: 来源: 题型:
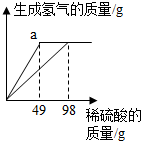 6.5 g锌分别与10%和20%的稀硫酸反应,反应中稀硫酸溶液的质量和生成氢气的质量关系如图所示.
6.5 g锌分别与10%和20%的稀硫酸反应,反应中稀硫酸溶液的质量和生成氢气的质量关系如图所示.
| 实验I | 实验II | |
| 锌的质量 | 6.5g | 6.5g |
| 稀硫酸的质量分数 | 10% | 20% |
查看答案和解析>>
科目: 来源: 题型:
| ||
. |
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量的熔融物于试管中,加入 |
固体全部溶解、有无色气体逸出、 |
熔融物含有铁和铝 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
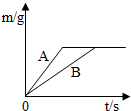 将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.对于该图象的理解,下列说法正确的是
将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.对于该图象的理解,下列说法正确的是查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 金属 | Ti | Al | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
查看答案和解析>>
科目: 来源: 题型:
|
|
|
| |||||||||
|
不 | 溶 | 溶 | 溶 |
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢 金属逐渐溶解 |
气体产生激烈金属迅速溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com