
科目: 来源: 题型:
取一段打磨好的镁带,放入白醋中,可以观察到的现象是( )
A.溶液由无色逐渐变为绿色 B.镁带发出耀眼的强光
C.镁带表面产生大量气泡 D.反应过程中释放出大量的热,使镁带熔化
查看答案和解析>>
科目: 来源: 题型:
每年的6月5日世界环境日,环境保护是我国的一项基本国策,空气的净化日益受到人们的关注。下列气体组中的各种气体都属于空气污染物的是( )
A.二氧化硫 一氧化碳 二氧化氮 B.二氧化碳 一氧化碳 氮气
C.氧气 二氧化碳 氮气 D.氮气 氧气 一氧化碳
查看答案和解析>>
科目: 来源: 题型:
下列实验操作不正确的是( )
A.点燃镁带必须用坩埚钳夹持,不能用手拿
B.实验过程中的废液应倒入水池,并用大量水冲刷
C.向试管中加铜绿粉末时可以用纸槽代替药匙加入药品
D.实验结束时要整理好实验台后方能离开实验室
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表
| 反应时间 | L0 | L1 | L2 | L3 |
| 烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 |
(1)反应中产生氢气_________g,这种钢样品中铁的含量是多少?(精确到0.1%)
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢。假设残留在烧杯中的黑色固体全部是炭,则这种钢属于_________________。
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻。可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多。原因是________________________。
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组设计的实验装置(如下图),既可用于制取气体,又可用于验证物质性质。
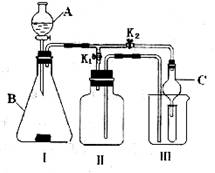
(1)写出仪器A和B的名称:A:_________;B:_________
(2)当打开K1、关闭K2时,利用Ⅰ、ⅡI装置可直接进行的实验是(填序号)。
①大理石与稀盐酸反应制取二氧化碳 ②锌与稀硫酸反应制取氢气
小颖认为在不改变Ⅰ、Ⅱ装置的仪器及位置的前提下,该装置可用于双氧水制取氧气,她的做法是_____________________________________________;
实验室还可以用高锰酸钾制取氧气,化学方程式为________________________________。
(3)当打开K2、关闭K1时,利用Ⅰ、Ⅲ装置可验证二氧化碳与水反应,生成了碳酸,此时试管中盛放的物质是_____________,可以观察到的现象是___________________________(C为干燥管,用于防止液体倒吸)。
查看答案和解析>>
科目: 来源: 题型:
某校化学研究性学习小组的同学在学习了《金属与矿物》一章后,做了如下图所示的探究实验。实验发现CO与CuO加热后黑色粉末变成红色粉末。请你参与该小组的研究过程并完成相关任务:
[研究课题]探究红色粉末的主要成分
[查阅资料]
(1)有关物质的颜色CuO粉末:黑色,Cu2O粉末:红色
(2)CuO和Cu2O都能和稀硫酸发生反应,化学方程式为:CuO十H2SO4=CuSO4+H2O
Cu2O+H2SO4=CuSO4+Cu+ H2O
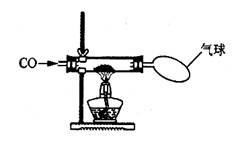
[猜想与实验]
(1)如果硬质玻璃管内红色粉末为一种物质,请猜想它的成分,并设计简单的实验证明你的猜测。
| 猜想 | 简单实验方案 | 现象 | CO和CuO反应的化学方程式 |
(2)如果硬质玻璃管内红色粉末为两种物质的混合物,要确定粉末中两种物质的质量分数,还需要通过有关数据计算进行判断。下列数据不可作为计算依据的是( )
A.反应前CuO粉末的质量 B.硬质玻璃管中固体物质减少的质量
C.通入CO的质量 D.反应后固体混合物的总质量
查看答案和解析>>
科目: 来源: 题型:
已知A~G七种物质都是初中化学课本中出现过的化合物,其中F是常用的建筑材料;H为常见的单质。各物质之间存在如下转化关系(反应条件如下图所示)。
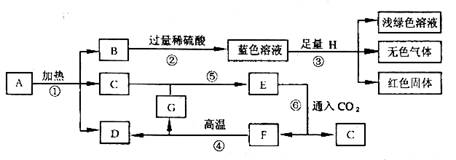
(1)请写出物质A的化学式___________________________。
上述蓝色溶液中的溶质有__________________、__________________。
(2)在①~⑥反应中属于化合反应的是__________________ (填序号)。
(3)上述转化过程中,有能够反映我国古代人民在化学方面对人类作出伟大贡献的变化。请举出其中一例,用化学方程式表示_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液。配制步骤为:
(1)计算:需氢氧化钠固体_________g,水_________mL(水的密度是1g/cm3)
(2)称量:用质量为23.1g的烧杯做称量容器,在托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在_______盘。在下表所列的砝码中,选出所需砝码(打“√”表示选用):
| 砝码/g | 100 | 50 | 20 | 20 | 10 | 5 |
| 打“√”表示选用 |
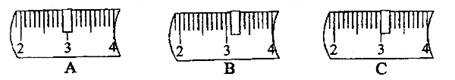
并在下列标尺中选出能正确表示游码位置的选项_________ (填字母).
(3)溶解:将氢氧化钠固体溶于水,用_________搅拌,使氢氧化钠全部溶解,冷却至室温。
(4)把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com