
科目: 来源: 题型:
活动小组同学通过Al、Fe、Cu三种金属与盐酸反应的实验,验证它们的活动性。
【所用药品】溶质质量分数相同的稀盐酸;大小和形状相同的铝、铁、铜
【实验记录】
| Al | Fe | Cu | ||
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速率慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速率快 | 产生气泡速率慢 | 无气泡产生 | |
【分析与结论】
(1)实验开始时铝表面几乎无气泡产生的原因是_______________________;
(2)铜表面始终无气泡产生的原因是________________;
(3)根据一段时间后三种金属与稀盐酸反应的现象,可证明三种金属的活动性由强到弱的依次是_______。
【拓展和应用】
(1)解释:在铁器表面常刷铝粉防锈的原因是____________________;
(2)判断:某酸雨多发地区,欲铸一座金属雕像,你认为选择以上三种金属中的_______为原材料更为适合;
(3)比较三种金属的活动性,除采用金属与酸溶液反应得方法外,还可以选用的方法是______(答一点即可)
【反思】在通过金属与酸溶液反应验证金属活动性的实验中,为确保实验成功,你认为应注意______________。(答一点即可)
查看答案和解析>>
科目: 来源: 题型:阅读理解
在日常生活中,我们发现切过咸菜的刀更容易生锈.而除锈用稀盐酸比稀硫酸快。为了进一步验证上述现象,某校师生做了以下相关分组实验,请你根据自己平时课堂学习的体验一起参与讨论并回答相关问题。
【步骤一】未打磨的铝片浸入氯化铜溶液中,迅速产生大量气泡和疏松的紫红色固体,并放热,片刻后溶液由蓝绿色变成无色。
(1)若要正视紫红色固体中是否含有氧化铜,可用_______溶液(填一试剂)加以检验。
【步骤二】未打磨的铝片浸入硫酸铜溶液中,一段时间内没有明显现象。
(2)比较步骤一、二,你能得出的结论是:_____________________。
【步骤三】打磨过的铝片浸入硫酸铜溶液中,其操作、现象和结论见下表。
(3)试将“影响因素”选项前恰当的字母序号填入答题卡指定位置。
| 实验操作 | 使用现象 | 对比结论 |
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 | 现象一与现象二对比,说明 ①______________ |
| 现象二:粗砂纸打磨的片刻内现象不明显。 | ||
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 | 现象三与现象一对比,说明 ②______________ |
| 现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象四与现象三对比,说明 ③______________ |
影响因素:A.打磨时用力程度及均匀程度不同;B.选用砂纸颗粒粗细程度不同;C.由于摩擦生热又形成了新的氧化膜
(4)比较步骤三各实验操作中用砂纸打磨的作用是:_____________________。
(5)请仔细观察下图:

试从微观粒子变化的角度分析该反应的实质是:______________。
查看答案和解析>>
科目: 来源: 题型:
酸与碱之间发生中和反应,其实质是酸溶液中大量自由移动的![]() 和碱溶液中大量自由移动的
和碱溶液中大量自由移动的![]() -结合成水分子的过程。请根据以下氢氧化钠溶液与稀盐酸反应的实验,回答问题。
-结合成水分子的过程。请根据以下氢氧化钠溶液与稀盐酸反应的实验,回答问题。
【实验1】用酚酞试液
(1)向一锥形瓶中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为_________色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为_________ (结果精确到0.1%)。反应后溶液中的溶质可用____________的方法(填一操作名称)使其析出。用酚酞作指示剂可逐滴控制酸、碱溶液反应的量,视觉效果灵敏,操作简便。
【实验2】用pH试纸
(2)向一支试管内倒入约2mL氢氧化钠溶液,再逐滴滴入盐酸,边滴边振荡。然后用玻璃棒蘸取反应液沾到pH试纸上,与标准比色卡对照。因无法通过肉眼观察到反应进程,需间隔数滴多次检测溶液的pH,所以每使用玻璃棒蘸取溶液前,必须进行_________的预处理。
【小结】
(3)除了用酸碱指示剂、pH试纸外,还可用_________ (填方法)检测中和反应是否发生。
查看答案和解析>>
科目: 来源: 题型:
2008年我省部分地区监测到的雨水平均pH如下表。请回答下列问题:
| 城市 | 广州 | 深圳 | 佛山 | 河源 | 肇庆 | 东莞 | 中山 |
| 2008年雨水平均pH | 4.47 | 4.8 | 4.54 | 6.37 | 4.86 | 4.83 | 4.58 |
(1)上表列举的7个地区中,没有酸雨污染的地区是_______;导致酸雨的主要气体是______(填序号):
①CO ②CO2 ③SO2 ④NO2 。
(2)若酸雨的主要成分为H2SO4和HNO3,请写出下列化学方程式:
(a)含H2SO4的酸雨腐蚀七星岩的石灰石_________________________________;
(b)含HNO3的酸雨与撒在田地里的熟石灰反应___________________________________。
(3)为了改善肇庆环境质量、迎接明年的“绿色亚运会”,下列措施不能减少酸雨的是__________(填序号):
①推广清洁能源 ②减少用煤直接作燃料 ③淘汰尾气不达标的汽车 ④限制燃放烟花爆竹 ⑤限制并有偿使用塑料袋。
查看答案和解析>>
科目: 来源: 题型:
下列各反应的化学方程式是否正确?如不正确,指出错在哪里?
(1)Cu+2HCl=CuCl2+H2↑
(2)Zn+2HNO3=Zn(NO3)2+H2↑
(3)2Fe+3H2SO4=Fe2(SO4)3+3H2↑
(4)Zn+2HCl=ZnCl2+H2↑
查看答案和解析>>
科目: 来源: 题型:
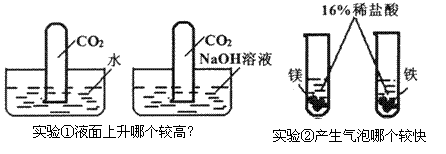
某校课外活动小组做了下列两组对比试验,请根据实验回答有关问题:
A B
(1)实验①中试管内液面上升较高的是_______(填字母);实验②中产生气泡较快的是_______(填字母)。
(2)实验①中试管内液面上升较高的反应的化学方程式是:____________________________
查看答案和解析>>
科目: 来源: 题型:阅读理解
小东对某农田的土壤酸碱性和改良方案进行研究。请填空:
取样:如右图所示在农田的四点,各取耕作层土壤约1 kg,让其自然风干,磨成粉状后混合均匀备用(以下称为土样)。

实验1 土壤酸碱性的测定
(1)实验目的:________________________;
(2)实验方法:取5g土样,放人碗底。加入自来水10mL,用玻璃棒充分搅拌均匀,待其静置澄清后,用玻璃棒蘸取清液到精密pH试纸(可精确到小数点后一位)上,即与标准比色卡比较,读出土样的pH;
(3)实验记录:进行二次实验,测得pH分别为:3.6、3.5、3.7;
(4)结果分析:
①从测定结果看,此土壤呈______ (填“酸”或“碱”)性;
②此实验方法有一处不够严密,请给予指出并改正:__________________;
实验2 用不同改良剂进行土壤改良的对比实验
(1)实验目的:研究不同改良剂对土样酸碱性的改变情况;
(2)实验方法:取三份土样各500g,分别加入0.2g不同改良剂和约l L左右的水,充分搅拌静置后,测定清液的pH;
(3)实验记录:见右表
| 加入的改良剂 | 重过磷酸钙 | 熟石灰 | 草本灰 |
| 有效成分化学式 | Ca(H2PO4)2 | Ca(OH)2 | K2CO3 |
| 测得的pH | 3.1 | 10.3 | 9.1 |
(4)结果分析:
①从本实验结果看,不能用于改良此土壤的改良剂是____________;
②为增强对比实验的说服力,在上述实验方法中,你认为对每种改良剂进行实验所加水量的要求应该是______;
实验3 改良剂用量的测定实验
(1)实验目的:研究使500g土样呈中性所需熟石灰的质量;
(2)实验方法:________________________________;
(3)此实验结果的作用是:___________________________。
查看答案和解析>>
科目: 来源: 题型:
在“世界环境日”活动中,某校化学兴趣小组对学校附近的一小型化工厂排出的无色废水进行探究。经调查发现该工厂在生产过程中用到盐酸。
[猜想]该工厂排放的废水呈酸性。
[设计实验]
| 实验操作 | 实验现象 | 实验结论 |
| 该废水呈酸性 |
[建议与反思]为防止造成水污染,同学们联合向厂家建议,应将废水治理达标后再排放,你认为治理该酸性废水时加入的试剂是____________(任答一种),此时废水的pH将__________(选填:“升高”、“不变”或“降低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com