
科目: 来源: 题型:
要除去下列物质中混有的少量杂质(括号内为杂质),所用的试剂和操作都正确的是( )
(A)CaCl2固体(CaCO3) 加足量稀硫酸、蒸发、结晶
(B)NaCl固体(Na2CO3) 加足量稀盐酸、蒸发、结晶
(C)Fe粉(Cu) 加足量稀盐酸、过滤、洗涤、干燥
(D)MnO2固体(KCl) 加足量水溶解、过滤、洗涤、干燥
查看答案和解析>>
科目: 来源: 题型:
A、B、C三只小烧杯内依次盛有一定体积的浓氨水、酚酞溶液、酚酞溶液,按图所示进行探究活动,不能得到的结论是( )
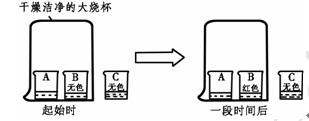
(A)氨分子是不断运动的
(B)碱能使酚酞溶液变红
(C)空气不能使酚酞溶液变红
(D)氨分子溶于水,形成的氨水使酚酞溶液变红
查看答案和解析>>
科目: 来源: 题型:
(1)H2O NaCl
(2)SO2 NO2等 AB
(3)①2H2O ==2H2↑+O2↑ ②CO2+H2O=H2CO3 ③CaO+H2O=Ca(OH)2 (②③答案可互换,且合理答案均给分)
(4)①能反应 ②3Fe+4H2O(g)==Fe3O4+4H2[‘‘(g)’’不写不扣分]
③b b处铁钉与水、空气同时充分接触(合理叙述均给分)
查看答案和解析>>
科目: 来源: 题型:
我们生活在“水球”上,地球表面的70.8%被水覆盖。
(1)海水晒盐是借助日光和风力使海水中的 (写化学式)蒸发,得到含有较多杂质的 (写化学式)晶体。
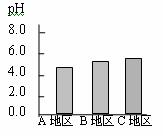
(2)降雨是自然界中水循环的一个环节。 气体或这些气体在空气中反应后的生成物溶于雨水,会形成酸雨。A、B、C三个地区雨水的pH如图所示,其中 地区的雨水是酸雨。
(3)请按要求写出初中化学教材中水作为反应物的化学方程式(两个化合反应中生成物的类别必须不同):
①分解反应:
②化合反应:
③化合反应: ![]()
(4)下表提供了在一定条件下.水能否与一些金属发生反应的信息。
①请根据金属活动性顺序和表中的已知信息,将表格填写完整。
| 物质 | 钠与冷水 | 镁与冷水 | 镁与水蒸汽 | 铁与冷水 | 铁与水蒸气 |
| 能否发生反应 | 剧烈反应 | 缓慢反应 | | 不反应 | 加热条件下能反应 |
②已知铁与水蒸气在加热条件下反应生成四氧化三铁和氢气.该反应的化学方程式为
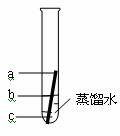
③铁虽然常温下与水不反应,但铁制品在潮湿的环境中容易生锈。某同学进行了如图所示实验。一周以后发现铁钉表面锈蚀。图中a、b、c三处锈蚀情况最严重的是 (填字母),产生该现象的原因是
查看答案和解析>>
科目: 来源: 题型:
(1)①16 184 ②左 BA 氢氧化钠易潮解(或氢氧化钠具有腐蚀性)
(2)①20g
②HCl、NaCl
③解:20g氢氧化钠溶液中NaOH的质量:20g×8%=1.6g
设该稀盐酸中HCl的质量为X
HCl+NaOH=NaCl+H20
36.5 40
X 1.6g
![]() =
=![]()
X=1.46g
稀盐酸的质量分数:![]() ×100%=7.3%
×100%=7.3%
答:该稀盐酸中溶质的质量分数为7.3%
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制200g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后 (按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是 .
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
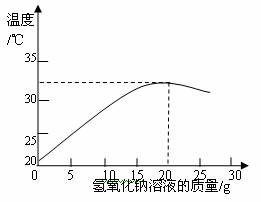
(2)右图表示用上述配制的氢氧化钠溶液与20 g某稀盐酸发生反应后溶液温度的变化情况。
①根据曲线判断,当加入氢氧化钠溶液的质量为 时,反应恰好完全进行。
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为 (写化学式)。
③试计算该稀盐酸中溶质的质量分数(请写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com