
科目: 来源: 题型:阅读理解
通过海水晾晒可得粗盐和母液,粗盐除NaCl外,还含有CaCl2、Na2SO4以及泥沙等杂质。海水可同时生产氯化钠和金属镁或镁的化合物等产品,其流程如下图所示:
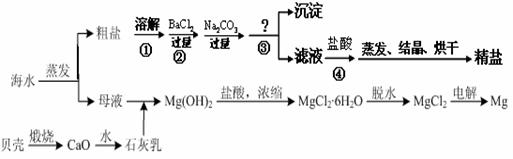
(1)制得粗盐和精盐的操作都包括蒸发步骤,有关其中“蒸发”步骤的叙述错误的是________。
a. 蒸发的目的是得到热饱和溶液 b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液 d. 应蒸发至有较多晶体析出时为止
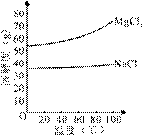
(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是_________。(填写“得到热饱和溶液”或“析出晶体”)
(3)在第①步粗盐溶解操作中要用玻璃棒搅拌,其作用是 ;第②步加试剂的目的是除去粗盐中的 (填化学式),第④步加入盐酸的目的是 。
(4)该流程的副产品中,除钙元素能被海洋生物利用外,还需综合利用的物质是_________。
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和水,其中MgO、MgCl2的物质的量之比为3:1,该反应的化学方程式为
;若不补充其它原料,还可制得溶质质量分数为_______%的盐酸。(计算结果精确到0.1)
(6)电解食盐水所得溶液中的溶质主要为氢氧化钠和氯化钠(其它溶质可忽略不计),已测得该溶液的密度为1.2 g/mL,为进一步测定其中氢氧化钠的含量,取该溶液样品25 mL与10%的稀硫酸反应,当加入49g稀硫酸时恰好完全中和。请根据化学方程式列式计算:
①25 mL该溶液样品中含氢氧化钠多少克?
②该溶液样品中氢氧化钠的质量分数是多少?
查看答案和解析>>
科目: 来源: 题型:
下图是一些气体的发生和收集装置,请按要求回答:
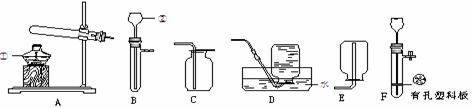
(1)若实验室以KClO3为原料制取O2,最适宜选择__________(填写仪器编号)进行组装。
(2)为了更好地制取CO2气体,有同学将B装置改进为F装置。改进后该装置的优点是__________________________________,该装置还可以制取的气体是 。
查看答案和解析>>
科目: 来源: 题型:
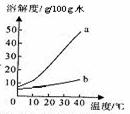
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线。
(1)Na2CO3溶解度曲线为 (填a或b)。
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
(2)要除去NaHCO3固体中的少量Na2CO3,应采用的物理方法是 (填写编号)。
Ⅰ. 冷却结晶 Ⅱ. 蒸发结晶 Ⅲ. 溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是 。
(4)40℃时的100.0g Na2CO3的饱和溶液中含有 g溶质,该溶液的溶质质量分数为 %,配制该溶液需要 g石碱和 mL水。(计算结果精确到0.1)
查看答案和解析>>
科目: 来源: 题型:
检验稀硫酸中混有稀盐酸,应选用的试剂是__________________ ,你的选用理由是 ,先后发生的反应是_______________________________________ (填写化学方程式)。
查看答案和解析>>
科目: 来源: 题型:
以下是探究水的组成的实验。右图是电解水实验的示意图:
(1)写出该反应的化学方程式 ;
(2)A端接电池 极(填“正”或“负”);
(3)电解水的过程中,发生改变的微粒是(写名称) ;
(4)该实验可证明水的元素组成,水是由(写名称) 组成的;
(5)水中元素存在形式是______________________(填“游离态”或“化合态”);
(6)检验B试管中气体的操作方法和现象是 ;
(7)若电解水消耗水3.6g,则A试管中生成气体的分子个数约为 ;
(8)为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验(装置如图),通过称量反应前后装置A、B的质量,结果测得 m(H)︰m(O)>1︰8,比理论值偏高,其原因可能是 。(填编号)
A.通入的氢气经过净化干燥 B.装置A内管口有水凝结
C.氧化铜没有完全还原 D.装置B同时吸收了空气中的水蒸气和CO2


查看答案和解析>>
科目: 来源: 题型:
小张用过量等质量锌粒分别与等体积的浓盐酸和稀盐酸在烧杯中进行反应,并绘制了烧杯中物质的总质量和反应时间关系的曲线(见右图),下列对曲线差异的解释错误的是( )
A.浓盐酸和稀盐酸与过量等质量的锌粒反应产生等质量的氢气
B.浓盐酸的浓度大于稀盐酸,同一时间内与锌反应产生氢气较多
C.浓盐酸的挥发性比稀盐酸强,氯化氢气体逸出使质量减少较多
D.浓盐酸密度大于稀盐酸,等体积的浓盐酸起始质量比稀盐酸大

查看答案和解析>>
科目: 来源: 题型:
已知某混合液由HCl、K2CO3、H2SO4、CuCl2、NaCl溶液中的几种混合而成,向该混合液中加Ba(OH)2溶液,产生沉淀量与加的Ba(OH)2溶液体积关系如右图。则下列说法不正确的是( )
A.该混合液中肯定没有K2CO3和H2SO4
B.沉淀完全时,消耗Ba(OH)20.4mol
C.F点溶液中的溶质肯定只有一种
D.F点和P点溶液中溶质的物质的量相等

查看答案和解析>>
科目: 来源: 题型:
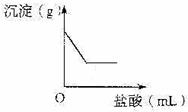
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、KNO3中的一种或几种。取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如右图所示。由此推断白色固体中( )
A.可能存在Na2SO4 B.可能存在KNO3
C.肯定不存在BaCl2 D.肯定只存在Na2CO3
查看答案和解析>>
科目: 来源: 题型:
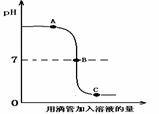
盐酸和氢氧化钠溶液(滴有酚酞试液)发生反应过程中溶液的pH变化如下右图。下列有关该实验事实的说法错误的是( )
A.该实验是将盐酸滴入氢氧化钠溶液中
B.B点表示盐酸和氢氧化钠恰好完全反应
C.B点和C点时,溶液均呈现无色
D.滴加硝酸银溶液,可证明发生了中和反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com