
科目: 来源: 题型:
杭州市的自来水由于增设了加臭氧(O3)和加活性炭两道处理程序,水质处于全国大城市优秀水平。根据以上报道,人们得出的下列结论中,符合科学道理的是
A.杭州市的自来水属于纯净物
B.杭州市自来水的物理、化学性质就是水的物理、化学性质
C.加臭氧和加活性炭都是利用它们的化学性质来净化水质
D.以上水处理过程中,水分子的化学性质不变[来源:学科网]
查看答案和解析>>
科目: 来源: 题型:
隔夜莱是否能吃,主要在于烧熟后的隔夜菜中亚硝酸盐含量的变化是否符合食品安全要求。蔬菜中的硝酸盐来自生长过程中所施氮肥。空气中的微生物(如硝酸盐还原菌)进入到蔬菜中,会产生一种还原酶,使蔬莱中的部分硝酸盐还原成亚硝酸盐。烧熟后的莱在食用和保存阶段都会有一些细菌进入;做熟的蔬菜更适合细菌生长。某研究小组对烧熟的莱中亚硝酸盐含量做了测试,数据如下表:
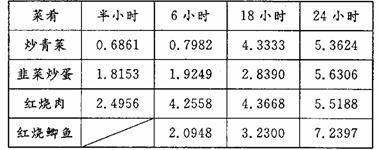
盖有保鲜膜的菜肴在40C的冰箱中放置不同时间的亚硝酸盐含量(单位:mg/kg)将一份红烧鲫鱼样本(不盖保鲜膜)在常温下放置4小时,测定其亚硝酸盐含量为8.9483mg/g。请根据以上材料,回答下列问题:
(1)亚硝酸盐中含有NO2-,其中氮元素的化合价是 价;
(2)根据表中的数据,莱中的亚硝酸盐含量变化的共同规律是 ;
(3)要使烧熟后的隔夜莱中亚硝酸盐含量尽可能低,保存的条件应该是 ;
(4)炒菜过程中温度一般在100℃以上,你认为从生莱炒到熟菜过程中的亚硝酸盐含量是否会持续增加 ,原因是 。
查看答案和解析>>
科目: 来源: 题型:
载人宇宙飞船内常用含氢氧化锂(LiOH是一种可溶性碱,具有碱的通性)的过滤网吸收宇航员呼出的CO2,以净化空气。若载人宇宙飞船内每名等航员平均每天呼出的CO2为550升,请回答:
(l)每天吸收一位宇航员呼出的CO2需氢氧化锂多少克?(列式计算,计算时CO2密度以ρ=2.0克/升计,相对原子质量:H 1;O 16; C 12; Li 7 Na 23)
(2)载人宇宙飞船使用的过滤网内选用氢氧化锂,而不用价格更便宜的氢氧化钠,其主要原因是
查看答案和解析>>
科目: 来源: 题型:
将一些能较好吸收和发射红外线的纳米级金属氧化物(如氧化铁、氧化铝、氧化锌等)通过特殊工艺织人纤维,然后用该种纤维制成的内衣,称之为红外保暖内衣。对于红外保暖内衣和普通保暖内衣在人体运动时,通气和散热的效果比较,某人设计如下实验:
①上午某时间穿红外保暖内衣,跳绳前测前胸体表温度,跳绳10分钟,再次测前胸体表温度。[来源:Zxxk.Com]
②下午某时间同一人穿普通保暖内衣(假设普通保暖内衣和红外保暖内衣除材质不同外,其余都相同),在通风状况相同的同一房间里,重复上午相同的实验步骤。
③比较上、下午跳绳前后的体表温度变化量,得出两种保暖内衣通气散热效果强弱结论。
请回答下列问题:
(1)洗涤红外保暖内衣时,不宜选用的洗涤剂是 (选填“弱酸性洗涤剂”、“弱碱性洗涤剂”、“中性洗涤剂”)
(2)若该人跳绳后腿部发酸,是因为肌肉细胞进行了
(3)有人认为根据该实验得出的结果不可靠,你认为该实验设计中变量控制不严密的地方是 、 ![]() (写两点)
(写两点)
(4)为了得出更可靠的![]() 结论,请写出你认为该实验最需改进的具体方面(写一点)
结论,请写出你认为该实验最需改进的具体方面(写一点)
查看答案和解析>>
科目: 来源: 题型:
雨、雪在形成和降落过程中吸收、溶解了空气中SO2及氮氧化物等物质,形成了pH小于![]() 5.6的降水称为酸雨,请回答下列有关酸雨的问题:
5.6的降水称为酸雨,请回答下列有关酸雨的问题:
(l)要测定某地采集到的雨水是否为酸雨,下列提供的试剂(试纸)中宜取用
A.蓝色石蕊试纸 B.紫色石蕊溶液 C.无色酚酞试剂 D.pH![]() 试纸
试纸
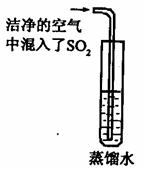
(2)已知 CO2的饱和溶液常温下pH不小于 5.6。通常空气中CO2的含量大于 SO2的含量,但人们反而将空气中的 SO2认定为形成酸雨的主要原因之一。有同学想通过如右图的实验寻找证据,你认为下一步的实验步骤是测定 ,只要出现 的实验结果,就可认定SO2溶于水有形成酸雨的可能。
(3)已知SO2与 CO2有许多化学性质是相似的,亚硫酸钙(CaSO3)是白色难溶于水但可溶于酸的固体。某同学向一酸雨样品中滴加 CaCl2,溶液本观察到有![]() 浑浊现象,继续滴入NaOH溶液后即有白色沉淀产生。在以上实验过程中,下列不可能发生的化学反应是
浑浊现象,继续滴入NaOH溶液后即有白色沉淀产生。在以上实验过程中,下列不可能发生的化学反应是
A SO2+CaCl2+H2O== CaSO3↓十2HCI
B.SO2+2NaOH==Na2SO3+H2O
C.![]() Na2SO3+CaCl2= CaSO3↓+2NaCI
Na2SO3+CaCl2= CaSO3↓+2NaCI
D.H2SO3 +2NaOH= Na2SO3+2H2O
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组通过如下实验由废铁屑制备硫酸亚铁晶体(FeSO4·7H2O):
①在洗涤过的废铁屑中加入适量稀硫酸,反应结束后过滤。
②将滤液转入到密闭容器中,静置、冷却析出硫酸亚铁晶体。
③待结晶完毕后,滤出晶体,用少量低温的水洗涤晶体3次。
请回答下列问题:
(1)在步骤①过滤时,所需用到的玻璃仪器中,除了漏斗、烧杯外,还需 。
(2)写出步骤①中发生反应的化学反应方程式
(3)步骤③中洗涤晶体用的水必须少量且低温,其原因是
(4)为了判断步骤③中晶体表面吸附的硫酸是否洗净,有人向第3次洗涤液中滴加硝酸钡溶液和稀硝酸,得到白色沉淀,以此证明该晶体并未洗净。该结论是否可靠?为什么?
查看答案和解析>>
科目: 来源: 题型:
有水(H2O)、双氧水(H2O2)、重水(D2O,“D”表示原子核中有一个质子和一个中子的氢原子)三种物质,从物质组成的角度看,这三种物质所含的元素共有 种,从化学性质的角度看, 与水的化学性质有较大的差异。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com