
科目: 来源: 题型:
下表列出了KNO3与NaCl在不同温度时的溶解度:
| 温度(℃) | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| KNO3的溶解度(g) | 13.3 | 20.9 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl的溶解度(g) | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(1)现有含123gKNO3与17.9gNaCl的混合物,某同学设计了以下实验除去KNO3中的NaCl(操作过程中不考虑额外的水损失).
①向混合物中加入适量水,加热溶解;学科王
②继续加热溶液至100℃并恒温蒸发浓缩;
③将溶液降温至10℃,仅得到KNO3晶体,过滤,将所得KNO3晶体洗涤并干燥.
A.步骤②中,为确保没有晶体析出,溶液中至少要保留 g水;
B.步骤③中,最多可得到KNO3晶体 g;
C.根据上述实验可概括出除去KNO3中少量NaCl的主要步骤:
加热溶解→蒸发浓缩→ →过滤→洗涤→干燥;
D.洗涤时,应选用少量 (选填“热水”或“冷水”).其目的是: ;
(2)除去NaCl中少量KNO3的一种方法是:将NaCl和KNO3的混合物置于适量水中,加热,搅拌,待KNO3全部溶解,趁热过滤,将过滤所得的NaCl晶体进行洗涤和干燥.上述方法中,趁热过滤的目的是:
(3)取23.4gNaCl和40.4gKNO3,加70g水,加热溶解.在100℃时蒸发掉50g水,维持该温度过滤,得到的晶体质量为 g;将滤液冷却至10℃,充分结晶,写出析出的晶体的化学式: .
查看答案和解析>>
科目: 来源: 题型:
如图是某浓盐酸试剂瓶上标签的部分内容.(1)将浓盐酸敞口放置,其质量分数会变小,这是由于浓盐酸具有较强的 ,所以浓盐酸必须密封保存;
(2)将该瓶浓盐酸全部配制成溶质质量分数为11.8%(密度约为1.06g/mL)的盐酸,需加入水 mL(ρ水=1g/mL);
(3)含杂质40%的石灰石100g与足量稀盐酸充分反应,理论上可得到CO2多少克?(假设杂质不与稀盐酸反应)

查看答案和解析>>
科目: 来源: 题型:
研究性学习小组利用如图所示实验装置进行了以下探究实验.步骤如下:
①检查装置气密性,加入锌粒和稀硫酸;
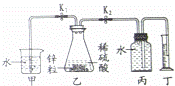 ②关闭K2、打开K1,待气泡连续均匀产生,立即关闭K1、打开K2,并开始计时;
②关闭K2、打开K1,待气泡连续均匀产生,立即关闭K1、打开K2,并开始计时;
③待丁中收集到10mL水,结束计时;
④换不同溶质质量分数、不同体积的稀硫酸,与质量相同的同一种锌粒重复上述实验;
⑤将每次实验的数据记录于下表:
| 硫酸用量(mL) | 40 | 40 | 20 | 20 | 20 | 10 | 10 |
| 硫酸的溶质质量分数(%) | 9.8 | 39.2 | 9.8 | 19.6 | 39.2 | 19.6 | 39.2 |
| 收集所用时间 | 4′03 | 1′36 | 4′12 | 3′30 | 1′40 | 3′42 | 1′48 |
(1)写出乙中反应的化学方程式: ;
(2)该实验的目的是:
(3)上述实验证明: 对该反应中氢气产生的速率有显著影响;
(4)若要快速制取大量氢气,可在乙中加入几滴硫酸铜溶液,但加入的量不可过多,原因是: (用化学方程式表示).
查看答案和解析>>
科目: 来源: 题型:
以下是今年我市实验操作考察的内容,请回答相关问题.
【实验目的】证明氢氧化钠溶液与稀盐酸发生了反应且生成了新物质;
【实验原理】 (用化学方程式表示);
【药品仪器】
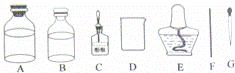
【实验步骤】
①取 (选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用 (填仪器名称)向①中溶液滴加稀盐酸,直至红色消失;
③向②中溶液继续滴加过量稀盐酸,溶液保持无色;
④用F蘸取③中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)步骤③的目的是: ;
(2)如不使用酸碱指示剂,进一步确认步骤④中的白色固体不是氢氧化钠的方法是: ;
(3)已知酚酞试液在不同pH时的变色情况如下表.某同学发现:向某氢氧化钠溶液中滴加酚酞试液后,溶液显无色;逐滴滴加稀盐酸,溶液先变红,后褪至无色.你认为该氢氧化钠溶液滴加酚酞试液显无色的原因可能是:
.请设计实验证明你的猜想(写出简要的操作步骤与现象:
| pH | <8.2 | 8.2~10.0 | >10.0 |
| 颜色 | 无色 | 红色 | 无色 |
查看答案和解析>>
科目: 来源: 题型:
用符合要求的物质的序号填空.
①氧气 ②浓硫酸 ③碳铵 ④熟石灰 ⑤聚乙烯
(1)实验中,可用作干燥剂的是: ;
(2)生产中,可用于制作食品包装袋的是: ;
(3)医疗上,在抢救危重病人时,用呼吸机输入的是: ;
(4)农业上,可作为肥料使用的是: .
查看答案和解析>>
科目: 来源: 题型:
(1)写出下列物质的名称、俗称或化学式.
| 名称 | 固态二氧化碳 | ② | 氢氧化钠 | 碳酸钠 |
| 俗名 | ① | 生石灰 | ③ | 纯碱 |
| 化学式 | CO2 | CaO | NaOH | ④ |
(2)判断下列物质的类别,并用相应的序号填空.
①单质 ②氧化物 ③酸 ④碱 ⑤盐
| 物质化学式 | KOH | SO2 | (NH4)2SO4 |
| 物质类别 |
查看答案和解析>>
科目: 来源: 题型:
将0.8g草酸亚铁(FeC2O4)放在一个可称量的敞口容器中加热灼烧,固体质量随温度升高而变化的数据如下(下表中所注明的各温度下,容器中的固体均为纯净物):
| 温度(℃) | 25 | 350 | 400 | 500 | 600 | 900 |
| 固体质量(g) | 0.80 | 0.80 | 0.40 | 0.44 | 0.44 | 0.43 |
下列叙述错误的是( )
①400℃时,容器中的固体为碳酸盐;
②400℃~500℃,发生了化合反应;
③600℃~900℃,发生的反应可表示为:6Fe2O3 ![]() 4Fe3O4 +O2↑
4Fe3O4 +O2↑
A.仅① B.仅①② C.仅①③ D.仅②③
查看答案和解析>>
科目: 来源: 题型:
向Fe(NO3)2、Mg(NO3)2和Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤.下列关于得到的溶液或滤渣的叙述正确的是(不考虑溶液中存在微量H+和OH—)( )
A.若滤液中含有Fe2+,则滤渣中一定不含Fe
B.若滤渣中含Cu,则滤液中一定含Fe2+
C.若滤渣中含Zn,则滤液中含2种离子
D.若滤渣中不含Zn,则滤液中至少含3种离子
查看答案和解析>>
科目: 来源: 题型:
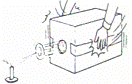
如图,在密封的纸盒上挖一个直径10cm的圆形小洞,并在洞口前方约1米的位置,放置一根点燃的蜡烛,用双手在纸盒两侧拍击,蜡烛熄灭.蜡烛熄灭的主要原因是( )
A.缺乏可燃物 B.缺乏O2
C.排出的气流中CO2的含量高
D.温度降到了可燃物的着火点以下
查看答案和解析>>
科目: 来源: 题型:
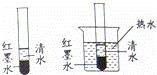
如图,向2支试管中分别加入等量清水和红墨水,使其有较明显的分界面,将其中1支试管放入盛有热水的烧杯中,观察到:浸在热水中的试管里的两种液体分界面模糊的更快些.该对比实验主要说明构成物质的微粒( )
A.体积小、质量小 B.在不断运动
C.相互之间有间隙
D.随温度升高运动速度加快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com