
科目: 来源: 题型:
(2011年山东威海,12题)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用PH计测定并记录反应过程中混合溶液PH 变化情况(如图所示).过滤后得滤液47.67g.请你计算,求出氢氧化钡溶液的溶质质量分数.可能用到的相对原子质量:H-1 0-16 S-32 Ba -137
查看答案和解析>>
科目: 来源: 题型:
(2011年浙江嘉兴,37题)如图所示,有人制作了一个家庭制氧装置。该制氧装
置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱。药剂包括过氧碳酸钠(2
Na2 C03·3 H2 O2)和二氧化锰。制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入
药剂:产生的气体通过B管从乙瓶导出,即可供人吸氧。
(1)为了顺利地导出甲瓶中产生的氧气,A软管在甲瓶中应 ▲ 。(选填“不伸入液面’’或“伸人液面")
(2)药剂加入水中后会发生以下两个反应: 2 Na2 CO3·3 H2O2=2 Na2 CO3+3 H2O2;
2H2 O22 H2 O+O2↑从化学反应的基本类型来看,它们都属于 反应。
(3)已知一包总质量为110克的药剂可34克过氧化氢,则这包药剂完全反应会生成多少克氧气?
查看答案和解析>>
科目: 来源: 题型:
(2011年江苏南通,25题)造纸是我国古代四大发明之一,它有效地推动了人类文明的发展。
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的______污染。秸秆的主要成分是纤维素[(C6H1005)n],纤维素中C、H、O三种元素的质量比为______(用最简整数比表示)。
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
①检测废水呈碱性的简单方法是_____。
②若某造纸厂废水中NaOH的质量分数为l.6%,现有废硫酸9.8 t(H2SO4的质量分
数为20%),可以处理的废水质量是多少?(计算过程写在答题卡上)
查看答案和解析>>
科目: 来源: 题型:
(2011年江苏泰州,27题)氯化钙钾石的化学式为KCl·xCaC12(x是CaCl2的系数)。它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液。某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如下图所示。请回答下列问题:
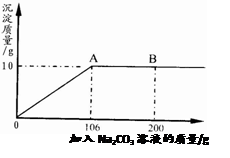
(1)写出Na2CO3与CaCl2反应的化学方程式 ▲ 。
(2)图中AB段表示的意义是 ▲ 。
(3)18.55g氯化钙钾石样品中:
①CaCl2的质量是 ▲ g;
②KCl的质量是 ▲ g;
③钾元素的质量分数是 ▲ 。
(4)所用N a2CO3溶液中溶质的质量分数是多少?(最后一问要求写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
(2011年山东聊城,8题)用“侯氏制碱法”制得的纯碱常含有少量的氯化钠(假定只含氯化钠杂质),某化学兴趣小组为了测量纯碱样品中碳酸钠的质量分数,做了如下实验:称量某纯碱样品12g,加入到足量的氯化钡溶液中,恰好完全反应.过滤干燥后,称得沉淀质量为19.7g.请计算:纯碱样品中碳酸钠的质量分数(计算结果精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
(2011安徽芜湖,16题)乙醇是一种清洁燃料,但在氧气不足时燃烧,会生成一氧化碳,现有207g乙醇与一定量的氧气点燃后发生如下反应:3C2H5OH+8O2点燃 XCO2+2CO+9H2O
(1)根据质量守恒定律可知:X= ;
(2)计算该反应生成一氧化碳的质量。
查看答案和解析>>
科目: 来源: 题型:
(2011年浙江金华,37题)氢气还原氧化铜实验得到的固体粉末为氧化铜和铜的混合物,科学兴趣小组的同学对该粉末中的单质铜的含量进行测定。三组同学各取10克粉末样品置于烧杯中,然后加入不同质量的同浓度的稀硫酸,充分反应后,对烧杯中剩余固体进行称量。实验数据记录如下:
| 组别 | 样品质量(克) | 加入稀硫酸质量(克) | 剩余固体质量(克) |
| 1 | 10 | 20 | 8.4 |
| 2 | 10 | 30 | 8 |
| 3 | 10 | 40 | 8 |
(1)分析表中数据可知,第2组实验中剩余固体是 。(写出物质名称或符号)
(2)样品中单质铜的质量分数为 。
(3)加入的稀硫酸溶质质量分数是多少?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
(2011年湖南怀化,30题)宇航员在太空舱中,往往可利用自己呼出的二氧化碳与过氧化钠粉末作用来获得所需的氧气,并合理处理呼出的二氧化碳。(反应方程式为2Na2O2+2CO2===2Na2CO3+O2)假如某宇航员在某次太空飞行中预计消耗氧气480kg,则该宇航员应在太空舱中至少准备多少克过氧化钠。(要求写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
(2011年湖南怀化,31题)根据右图浓盐酸的商标,回答下列问题
(1)某研究小组的同学欲用该盐酸配制100g10%的稀盐酸,需该盐酸 g(保留一位小数),配制时应选用 (填“10ml”或“50ml”)量筒量取。
(2)小组同学用所配制稀盐酸来测量水垢【主要成分为CaCO3和Mg(OH)2】中CaCO3的质量分数:取10.0g水垢,加入所配100g10%的稀盐酸中,测得各时间段内生成气体的质量如下表:
通过实验,计算该水垢中CaCO3的质量分数。
查看答案和解析>>
科目: 来源: 题型:
(2011年山东潍坊,26题)钢铁的生产和使用是人类文明和社会进步的一个重要的标志。
(1)每年钢铁锈蚀都会造成巨大的损失,铁制品锈蚀的主要原因是
。
(2)校课外兴趣小组的同学们去潍坊某钢铁长生铁样品进行实验:将四份不同质量的生铁样品(假定其中只含单质铁和单质碳)分别加到100g质量分数相同的稀硫酸中,充分反应后,测得的实验数据如下表(已知:在标准状况下,22.4LH2的质量为2g)
| 实验序号 | 1 | 2 | 3 | 4 |
| 生铁样品的质量 / g | 2.88 | 5.76 | 9.24 | 10.28 |
| 生成H2的体积(标准状况下)/L | 1.12 | 2.24 | 3.36 | m |
通过计算回答下列问题:
①上述表格中m的值为 。
②根据表中数据计算稀硫酸中H2SO4的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com