
科目: 来源: 题型:
2012年3月6日,包括圆明园兽首在内的一批珍贵文物首次在烟台展出。小霞看到这些240年前的铜质兽首后,她想探究铜是怎么冶炼出来的。
【查阅资料】(1)冶炼铜可以用常见的铜矿石——孔雀石,其主要成分是碱式碳酸铜[Cu2(OH)2CO3]。碱式碳酸铜是一种绿色的不溶于水的固体,加热易分解,能与酸反应。Cu2(OH)2CO3 2CuO+CO2↑+H20, Cu2(OH)2CO3+4HCl===2CuCl2+CO2↑+3H2O。
2CuO+CO2↑+H20, Cu2(OH)2CO3+4HCl===2CuCl2+CO2↑+3H2O。
(2)实验室可以用至少三种方法来制取铜:①用氢气在加热的条件下还原氧化铜(生成铜和水);②电解氯化铜溶液(生成铜和氯气,氯气有毒);③用活泼金属从铜的盐溶液中置换。
【设计方案】在实验室中以碱式碳酸铜、铁粉、稀盐酸为原料来制取铜。请你仿照下图①帮她画出另外两种制取铜的流程图。
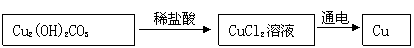 ①
①
②
③
【反思评价】(1)上述三种制取铜的方案中,你认为最理想的是_________,与其他两种方案比较,它有哪些优点(至少答一点):_______________________
__________________________________________。
(2)铜锈的主要成分也是碱式碳酸铜[Cu2(OH)2CO3]。铜生锈除了与空气中的氧气和水关外,从碱式碳酸铜的化学式推知,还可能与空气中的____________有关。
查看答案和解析>>
科目: 来源: 题型:
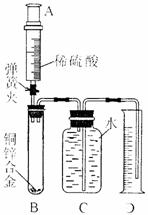
某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置
已略去)
探究过程如下:
1.连接实验装置并检查装置气密性
Ⅱ.向B中加入质量为m的铜锌合金粉末,由注射器A向B
缓缓加入稀硫酸,待B中不再有气体产生气体时,夹紧弹簧夹,
立即移出D中导管,准确读取并记录量筒内水的体积。
Ⅲ.经过滤等操作,准确称量并记录B中剩余固体物质的
质量。
IV.该小组的甲同学根据反应前后B中固体物质的质量计
算样品中锌的质量分数;乙同学认定量筒内测得水的体积
即为反应生成气体的体积,并利用该气体在常温下的密度,根据化学方程式进行相关计算,得到样品中锌的质量分数。
请回答下列问题:
(1) B中发生反应的化学方程式是
。
(2)Ⅲ中,正确的操作顺序是:过滤、 、 、称量。
(3)通过误差分析,化学小组发现乙同学所用数据不可靠。造成该数据不可靠的原因及其对计算结果的影响是:
 ①II中,移出D中的导管内留存有水,导致计算结果偏小。
①II中,移出D中的导管内留存有水,导致计算结果偏小。
② ,导致计算结果偏 。
……
查看答案和解析>>
科目: 来源: 题型:
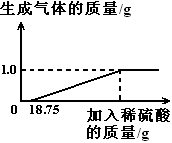
某兴趣小组对生锈废铁锅中铁的含量进行了测定。生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应)。兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示。
(1)从化学元素与人体健康的角度考虑,我们应选用铁锅还是铝锅 ,为什么 。
(2)废铁锅片中铁单质的质量分数为 。(结果保留到0.1%)
(3)所得溶液中所含溶质的化学式为 ,计算溶液中硫酸铁的质量。
(要求写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物。
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气。
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
【氢化钙的制备】
氢化钙通常用氢气与钙加热制得。某化学兴趣小组设计的制取装置如图10所示(固定装置省略)。
 回答下列问题:
回答下列问题:
(1)装置A中制取氢气的化学方程式为 。
(2)装置B的作用是 。
(3)装置C中制取氢化钙的化学方程式为 。
(4)若不改变温度,整套装置气密性的检查方法是 。
【产品的定量测定】
通过上述方法制得的氢化钙样品中常混有未完
全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
①检查装置气密性,装入药品,按图11(固定
装置省略)所示连接仪器。
 ②调整水准管高度,使量气装置两边的液面保持
②调整水准管高度,使量气装置两边的液面保持
同一水平。读取液面所在的刻度数据为10.0 mL。
③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合。
④反应结束,冷却至室温,再次读取液面所在刻度数据为110.0 mL。
回答下列问题:
(5)如何判断样品与水完全反应: 。
(6)反应生成氢气的体积为 mL。
(7)已知该实验条件下,氢气的密度为0.09 mg/mL。
样品中氢化钙的纯度为 。(结果精确到0.1%)


查看答案和解析>>
科目: 来源: 题型:
 做“镁带在空气中燃烧”实验时,小科同学发现生成物中有少量黑色固体。黑色固体是镁和什么物质反应所产生的?他提出下列猜想:
做“镁带在空气中燃烧”实验时,小科同学发现生成物中有少量黑色固体。黑色固体是镁和什么物质反应所产生的?他提出下列猜想:
猜想一:黑色固体可能是镁和氮气反应的产物;
猜想二:黑色固体可能是镁和二氧化碳反应的产物。
为了验证上述两个猜想,小科设想:
(1)让空气通过A、B装置,其中A装置的作用是 ;
(2)用C瓶收集通过A、B装置后的气体,并加入足量的红磷燃烧;待C瓶冷却后,再把点燃的镁带放入C瓶中。
经过思考发现,由于收集气体时相关气体的密度差异及C瓶冷却后瓶内外的气压差异,达不到预期效果。
于是,他在老师的帮助下获得了这种气体,观察到镁带在该气体中燃烧并有淡黄色的固体产生;然后用D瓶收集一瓶 气体,把点燃的镁带放入D瓶中,观察到镁带在D瓶也能燃烧,同时有白色和黑色固体生成。
通过以上实验,凶得出结论:猜想 正确。同时,他对燃烧有了新的认识:
。
查看答案和解析>>
科目: 来源: 题型:阅读理解
某化学兴趣小组的学生,发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行如下探究活动:
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R,猜想二: ,猜想三:R> Al>Cu,
【查阅资料】 R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色。
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究。
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一 (填“成立”或“不成立”) |
| 猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立。 R与稀硫酸反应的化学方程式为
|
| 猜想三 |
| 无明显现象 | 猜想三成立 |
 【交流反思】
【交流反思】
究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误。于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色 ;进而确认猜想三不成立,猜想三成立。
【归纳总结】探究结束后,他们总结得出:通过金属与 反应或金属与 反应可以比较金属活动性强弱。
查看答案和解析>>
科目: 来源: 题型:阅读理解
钢铁工业是国家工业的基础。
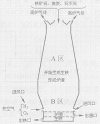
(1)右图是教材中炼铁高炉及炉内化学变化过程示意图,
根据图示回答下列问题。
若右图中采用的铁矿石的主要成分为氧化铁,请写
出A区和B区所发生主要反应的化学方程式:
A区
B区
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。
[设计实验]
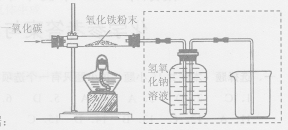
用一氧化碳还原纯净的氧化铁
粉末,实验装置如右图。
[进行实验]
该小组按上述实验设计,在一定
温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
 [分析与讨论]
[分析与讨论]
本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部
是铁,但小华同学提出了质疑,于是大家提出查阅资料。
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关。
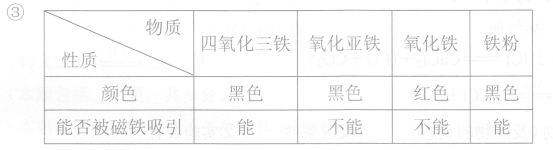
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁。
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和————。
②进行猜想:黑色固体粉末可能
a.全部为铁 b. c 。
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称) 。
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间。
②实验装置图中采用虚线框内的装置,其作用有 。
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳
查看答案和解析>>
科目: 来源: 题型:
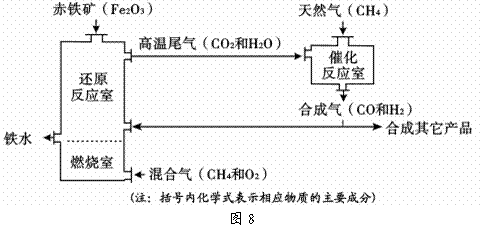
竖炉冶铁工艺流程如图8所示。
 |
回答下列问题:
(1)该工艺流程中,甲烷的作用是 ,冶炼出的铁水属于 (填“纯净物”或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理 。(写一个)
(3)该工艺流程中,可循环利用的物质是 。
查看答案和解析>>
科目: 来源: 题型:
早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空:

(1)写出CO还原Fe2O3的化学方程式 ;
(2)实验中盛澄清石灰水的试管中可观察到的现象是 ;
(3)右边导气管口放置点燃的酒精灯的目的是 ;
(4)实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是 。
查看答案和解析>>
科目: 来源: 题型:
暖宝宝是一种防寒用品,如图所示。暖宝宝中的主要成分有哪些?发热的原因是什么?

(1)小明探究:暖宝宝中的主要成分是什么?
剪开内包装袋,倒出其中的粉末,发现呈黑色。
【提出猜想】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化
三铁中的一种或几种。
【初步验证】将磁铁靠近黑色粉末,部分被吸引。
【查阅资料】四氧化三铁具有磁性,能被磁铁吸引。
【得出结论】该黑色粉末可能含有 。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取黑色粉末加足量稀硫酸 | 固体部分溶解,有气泡产生,溶液无蓝色 |
| ② | 取实验①的残渣灼烧,将内壁涂有 澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
由实验①可知,该黑色粉末肯定含_____________,肯定不含______________. ;写出实验①的化学反应方程式_________________________。
由实验②可知,该黑色粉末肯定含 。(2)小明思考:暖宝宝为什么会发热?
【查阅资料】暖宝宝中的铁粉在空气中发生了缓慢氧化,进而放出热量。
由此可见,人们可以利用化学反应放出的能量,请再举一例:___________________。(3)人们利用化学反应还可以_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com