
科目: 来源: 题型:
反思、归纳与提升是化学学习的重要方法。对于复分解反应及其规律,通过反思与探索,同学们有了新的认识。请填写下文中横线上的空白。
【知识回顾】
1.氯化氢气体、氢氧化钠固体不导电。
2.盐酸、氢氧化钠溶液能导电


【迁移运用】硫酸钠溶液能导电,原因是硫酸钠溶于水:Na2SO4→________。
【探索发现】
(1)氢氧化钠溶液与盐酸反应的微观示意图


(2)硫酸钠溶液跟氯化钡溶液反应的微观示意图


(提示:生成硫酸钡白色沉淀)
(3)有气体生成的复分解反应,以Na2CO3+2HCl=2NaCl+H2O+CO2↑为例,反应实质:2H++CO32-→________________。
【总结规律】
上述复分解反应能发生的本质原因____________________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究。
[查阅资料]
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
[实验探究]
(1)探究两者水溶液酸碱性的差异
 小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变 ▲ 色,但食用纯碱溶液中颜色更深,由此推测可能 ▲ 溶液碱性更强。小欢认为要比较两种溶液的碱性强弱,可直接用 ▲ 进行测定。
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变 ▲ 色,但食用纯碱溶液中颜色更深,由此推测可能 ▲ 溶液碱性更强。小欢认为要比较两种溶液的碱性强弱,可直接用 ▲ 进行测定。
(2)验证两种粉末的稳定性
在老师的指导下,该小组按右图装置进行实验操作,观察到 ▲ (填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为 ▲ ,装置中棉花的作用是 ▲ 。
(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用右图装置进行实验测定。
 数据记录如下:
数据记录如下:
| 称量项目 | 称量时间 | 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
(5)反应生成CO2的质量为 ▲ g。
(6)通过计算确定食用纯碱粉末中Na2CO3的质量分数。(写出计算过程,结果保留一位小数。)
③ 如果测得的结果比实际纯度高,可能的原因是 ▲ 。(答一种即可)
查看答案和解析>>
科目: 来源: 题型:
某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
(1)小红同学从某一欠收农田里取回一份土壤样品,如果检测结果呈酸性,从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加 (填化学式)。
 (2)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。
(2)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。
I.为了验证反应①,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成 。
II.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为: 。
III.为了验证反应③能够发生,你选择的物质是 。
a.Na2CO3 b.HCl c.FeCl3 d.Ba(NO)2
(3)请你设计一个实验除去FeCl2溶液中少量的CuCl2,写出主要操作步骤和化学方程式:
实验主要操作步骤: 、 , 化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D四种化合物分别通过分解反应生成两种物质,如下所示(反应条件略去):① A → B + M ② B → M + N ③ C → M + P ④ D → M + Q
在生成物中N被认为是最清洁的燃料,P是常温下为液态的金属,Q的水溶液跟硝酸银溶液反应生成一种不溶于稀硝酸的白色沉淀,试推断(用化学式表示):
(1)A是 B是 C是 D是
(2)写出②对应的化学方程式
写出Q的水溶液跟硝酸银溶液反应的化学方程式
; 反应类型
查看答案和解析>>
科目: 来源: 题型:
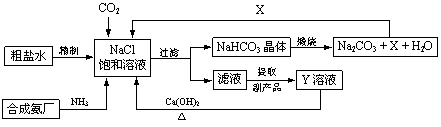
我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:
 |
| 部分物质溶解性(室温) | |||
| OH- | SO42- | CO32- | |
| Mg2+ | 不 | 溶 | 微 |
| Ca2+ | 微 | 微 | 不 |
| Ba2+ | 溶 | 不 | 不 |
⑴粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制。则加入试剂合理的顺序为 、盐酸(只写一种)。加盐酸的作用是(用化学方程式表示) 、 。
⑵制碱原理为:NaCl + CO2 + NH3 + H2O = NaHCO3↓+ NH4Cl,该反应原理可看作是由①CO2 + NH3 + H2O = NH4HCO3和②NaCl + NH4HCO3 = NaHCO3↓+ NH4Cl两个反应加合而成,则的反应类型为 。
⑶X的化学式为 。
⑷Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为 ,Y的化学式为 ,写出Y的一种用途 。
查看答案和解析>>
科目: 来源: 题型:
某碳酸钠样品中含有少量氯化钠杂质,为测定该样品中碳酸钠的质量分数,进行了如下实验:

请回答下列问题:
(1)操作A用到的玻璃仪器除烧杯外还必需有 ;
使用托盘天平进行称量前,应先检查 。
(2)在实验过程中加入饱和石灰水后发生反应的化学方程式是
。
(3)为探究上述反应后滤液中的溶质成分,甲同学向滤液中滴加过量稀盐酸,发现
有气泡产生,则滴加盐酸前滤液中的溶质除氯化钠外还有 ;滴加盐酸的过程中发生反应的化学方程式为
。
查看答案和解析>>
科目: 来源: 题型:
(2012·泸州)有A、B、C三种化合物,已知A是强酸,B是硝酸盐,C是强碱,它们都溶于水,能发生以下反应,B、C混合,生成蓝色沉淀;A、C混合,生成难溶于稀硝酸的白色沉淀E。是推断:B的化学式为 ,C的化学式为 ,E的化学式为 。
查看答案和解析>>
科目: 来源: 题型:
实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵 (NH4C1)和尿素[CO(NH2)2]中的一种。为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下实验(此处箭头表示得出实验结论):

根据上述实验回答:
(1)写出三种化肥的名称:A ;B :C 。
(2)如果实验II中B、C两种样品没有另取,对实验结果— —(填“有”或“无”)影响。
(3)常温下如要鉴别B、C两种样品, (填“能”或“不能”)采取闻气味的方法。
(4)由实验和查阅资料可知,。人们在施用铵态氮肥时,若遇到碱性物质,会使铵态氮肥转化为氨气,氨气进入大气后与雨水作用,可能形成“碱雨”。“碱雨”中碱的化学式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com