
科目: 来源: 题型:解答题

 实验,得到图2中曲线c.
实验,得到图2中曲线c.查看答案和解析>>
科目: 来源: 题型:解答题
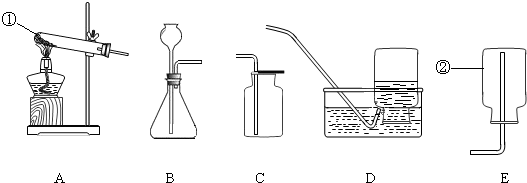
查看答案和解析>>
科目: 来源: 题型:单选题
 Al2O3+AlCl3+3NO↑+6X↑,则X的化学式为
Al2O3+AlCl3+3NO↑+6X↑,则X的化学式为查看答案和解析>>
科目: 来源: 题型:单选题
| 事实 | 解释 | |
| A. | 花香四溢 | 分子不断的运动 |
| B. | H2O2能杀菌消毒而H2O则不能 | 两种物质的分子构成不同 |
| C. | 温度计中的水银(汞)热胀冷缩 | 原子的大小发生改变 |
| D. | KMnO4和K2SO4 溶液的颜色不同 | 两种溶液中的阴离子不同 |
查看答案和解析>>
科目: 来源: 题型:解答题
地球“发烧”了
材料1.空气的成分
空气是多种气体的混合物.空气的成分可分为恒定成分和易变成分两类.恒定成分是指在空气中含量大,在任何地方含量几乎不变,包括78.06%氮气、20.94%氧气、0.94%氩等稀有气体,合计约占99.94%.易变成分是指在空气中含量很少,但因季节、地域等自然因素和人类的活动而引起相对含量的较大变化,甚至某些成分急剧增加或减少.下表中列出了大气中几种易变成分:
| 易变成分(浓度cm3/m3) | 变化的原因 |
| 二氧化碳 约300(约占空气的0.03%) | |
| 水蒸气 约290(约占空气的0.03%) | |
| 甲烷 约1.0~1.2 t | 天然气泄漏 |
| 氮的氧化物约0.52 | 化石燃料的燃烧 |
| 臭氧 0.01~0.04 | 含氟化合物的使用 |
| 硫的化合物:二氧化硫、硫化氢等 | 化石燃料的燃烧等 |
| 一氧化碳 | 汽车尾气等 |
| 合计:0.06% |
材料2.自然界中碳循环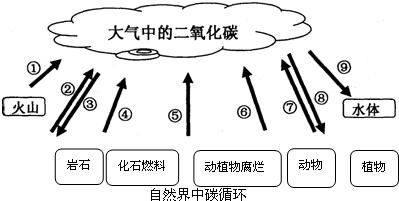
试回答下列问题:
(1)从地球上动植物生命活动所需要的物质角度看,为什么空气如此重要?(答出3条即可)________
(2)大气中多余的二氧化碳从何而来?
从上述材料可以看出,人类赖以生存的大气,正遭受空前严重的破坏.二氧化碳作为一种主要的温室性气体,含量增加导致气候变暖、地球“发烧”、灾害频发,成为当前威胁人类生存发展最严重的问题.分析材料2,你认为导致大气中二氧化碳含量增加的直接原因是(写出两条即可)________;
在②中,以石灰石为例,分解反应的化学方程式为________.
在⑧中,消耗二氧化碳的过程叫做________.在⑨中,消耗二氧化碳反应的化学方程式为________.在④中,以天然气为例,燃烧反应的化学方程式为________.
(3)如何除去大气中多余的二氧化碳?
据统计,大气中每年新增CO2约为l85~242亿吨,而其综合利用还不足l亿吨/年,仅靠碳的自然循环来平衡大气中二氧化碳已不可能.为了降低大气中二氧化碳的含量,化学家们正想尽办法用化学反应的手段使二氧化碳“变废为宝”.
①火电厂用碱液吸收产生的二氧化碳,获得化工产品碳酸钠.该反应的化学方程式为________.
②日本科学家研制成功一种新型催化剂,在常压、300℃条件下,CO2和H2反应生成甲烷和水.该反应的化学方程式为________.
③用三甲基膦做催化剂,在高压、极低温度条件下,CO2和H 2可以高效合成甲酸(HCOOH),并实现了工业化生产.该反应的化学方程式为________.
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com