
科目: 来源: 题型:
下列有关知识的叙述中,不正确的是
A.绿色化学的核心是要利用化学原理从源头上减少和消除工业生产对环境的污染
B.玻璃是一种硅酸盐材料,在日常生活和生产中具有重要作用
C.只由一种元素组成的物质属于单质,有不同元素组成的物质属于化合物
D.酸溶液中都含有氢离子,因此酸具有相似的化学性质
查看答案和解析>>
科目: 来源: 题型:
生活、生产中处处离不开化学知识,下列说法中,错误的是
A.用煤炉取暖在屋里洒水可防止煤气中毒 B.废旧电池中的化学物质能严重污染环境
C.煤井中要严禁烟火防止瓦斯爆炸 D.用生石灰处理含酸量超标的工业污水
查看答案和解析>>
科目: 来源: 题型:
化学是一门以实验为基础的学科,以下实验操作中,不合理的是
A.浓硫酸沾到皮肤上,应立即用大量的水冲洗,然后涂上3%-5%的碳酸氢钠溶液
B.点燃或加热氢气等可燃性气体时,必须先检验气体的纯度
C.用托盘天平称量药品时,先调节天平平衡,后称量
D.为了防止液体流出,将胶头滴管紧贴试管内壁滴加液体
查看答案和解析>>
科目: 来源: 题型:
近期饮食安全成为大家非常关心的话题,下列有关做法中,合理的是
A.用苏丹红等制作咸鸭蛋 B.将病死鸡禽放入冷库择机出售
C.种植草莓超量使用膨大剂和增甜剂 D.加入适量小苏打焙制糕点
查看答案和解析>>
科目: 来源: 题型:
造纸是我国古代四大发明之一,它有效地推动了人类文明的发展。
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的 污染。秸秆的主要成分是纤维素[(C6H10O5)n],纤维素中C、H、O三种元素的质量比为 (用最简整数比表示)。
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
①检测废水呈碱性的简单方法是 。
②若某造纸厂废水中NaOH的质量分数为l.6%,现有废硫酸9.8 t(H2SO4的质量分数为20%),可以处理的废水质量是多少?(计算过程写在答题卡上)
查看答案和解析>>
科目: 来源: 题型:
科学家经过研究,发现二氧化碳也是一种宝贵的碳氧资源。以CO2和NH3为原料合成尿素[CO(NH2)2]是固定和利用CO2的成功范例。它还可以与氢气反应生成多种有机物,如甲烷(CH4)、乙烯(C2H4)等。试计算:
(1)CH4中碳、氢元素的质量比 。
(2) CO(NH2)2中氮元素的质量分数 。(计算结果精确到0.1%)
CO(NH2)2中氮元素的质量分数 。(计算结果精确到0.1%)
(3) CO2转化为C2H4的化学方程式为:2CO2+6H2一定条件C2H4+4H2O,若用24gH2转化CO2,则理论上能生成C2H4多少克(列式计算)?
查看答案和解析>>
科目: 来源: 题型:
已知:①金属钠是一种活泼的金属,与水反应生成氧氧化钠和氢气;②难溶于水的碱受热分解生成相应的氧化物和水。A、B、C、D、E、F、G、H是初中化学中常见的物质,甲、乙、丙是三种金属。其中甲最活泼,乙是红色金属,丙能被磁铁吸引。各物质间相互转化关系如下图:
请回答下列问题:

(1)写出A、E、G的化学式:A ,E ,G 。
(2)操作X的名称是 。
(3)①无色溶液D与蓝色溶液F反应的化学方程式为 _________________________;
②金属甲与无色液体A反应的化学方程式为 ______________________ ,该反应的基本类型 ;
(4)甲、乙、丙三种金属的活动性由强到弱的顺序是 _________ ,无色气体C在点燃或加热前必须进行的操作是 ___________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体。某研究性学习小组对蓝色固体的成分进行了如下探究。请完成下列各题:
(一)猜想与假设:
猜想一:固体为CuCO3,理由: _____________________(用化学反应方程式表示)。
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈 (填“酸”或“碱”)性。
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2 、CuCO3受热易分解,各生成对应的两种氧化物。
、CuCO3受热易分解,各生成对应的两种氧化物。
(三)设计与实验:
Ⅰ.固体的获取:
(1)将反应后的固、液混合物经 、洗涤、低温烘干得 蓝色固体。
蓝色固体。
(2)判断固体已洗净的方法及现象 ________________________________________。
Ⅱ.用下图所示装置,定性探究固体的成分。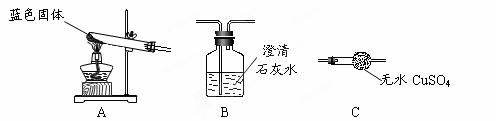
(3)若用装置A、B组合进行实验,B中无现象,则猜想 正确;
(4)若用装置A、C组合进行实验,C中无现象,则猜想 正确;
(5)小组同学将装置按 A、 、 (填“B”、“C”)的顺序组合进行实验,验证出猜想三是正确的,实验中:B中的现象为 ______________________,C中的现象为 ___________________________________。
结论:固体为Cu(OH)2和CuCO3的混合物。
Ⅲ.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃。设固体的组成为aCu(OH)2•bCuCO3。小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如右图,请根据图示回答下列问题:
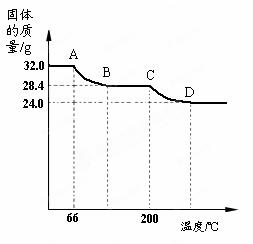
(6)写出A B、C D段发生反应的化学方程式: AB段: ____________________ ; CD段: __________________________ ;
(7)通过计算可得: a:b= 。
(8)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式: _________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com