
科目: 来源: 题型:
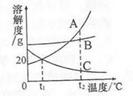
溶液在生产和生活中有着重要意义,如图是A、B、C
三种固体物质的溶解度曲线,请回答下列相关问题:
(1)t2℃时,A、B、C三种物质的溶解度从大到小
的顺序是 ;
(2)将t1℃时A、B、C三种物质的饱和溶液升温到t2℃,
所得溶液中溶质的质量分数最小的是 。
查看答案和解析>>
科目: 来源: 题型:
根据固体物质M在水中的溶解度曲线图,回答下列问题:
(1)B点所表示的溶液为M在t2℃的 (选填“饱和”或“不
饱和”)溶液。
(2)将A点对应的溶液从t1℃升温到t2℃(忽略水的蒸发),在此过程中M的质量分数 (选填“增大”、“减小”或“不变”);
(3)将A点对应的100 g溶液恒温蒸发10 g水,可析出M的质量为 g,剩下的溶液中M的质量分数为 。

查看答案和解析>>
科目: 来源: 题型:
水是一种重要的自然资源,与人类的生产、生活密切相关。
(1)降雨是自然界中水循环的一个环节,请用分子运动的观点解释这一变化过程
。
(2)pH<5.6的降水称为酸雨,要检验某次降水是否是酸雨,正确的操作为:
。
(3)水是常用的溶剂。向20mL水中溶解一定量KNO3固体的操作如下,请根据实验现象和溶解度曲线回答下列问题(水的密度以1g/mL计):

A、B、C中溶液一定是饱和溶液的是 ,一定是不饱和溶液的是 ;
当X= g时,B中恰好没有固体剩余。
查看答案和解析>>
科目: 来源: 题型:
某实验小组对不同条件下的硝酸钾的溶解情况进行了以下实验。
在甲乙丙三个烧杯中放入20g硝酸钾晶体,再分别加入50.0g冷水、热水与酒精,充分搅拌后(保持各自的温度不变),结果如下图所示。

(1) 甲烧杯中溶液是 (填“饱和”或“不饱和”)溶液。
(2) 由以上实验可得出结论:影响物质溶解度的因素有_______、__________.
(3) 将乙烧杯中的溶液降温到t2。C时,硝酸钾的溶解度是______g/100g水。再往乙烧杯中加入10g水,改变温度至t2 C时,溶液又恰好达到饱和状态,则t1____t2(填“>”、“<”或“=”)。
(4)  经实验测定,获得不同温度时硝酸钾的溶解度数据。
经实验测定,获得不同温度时硝酸钾的溶解度数据。
| 温度 | 溶解度(g/100g水) |
| 20 | 31.6 |
| 40 | 63.9 |
| 50 | 14 |
| 60 | 110 |
| 70 | 140 |
| 80 | 169 |
分析上述数据,某温度时的硝酸钾溶解度数据可能存在较大的误差,该温度时________。C.
请根据表中的数据,在坐标图中描点、绘制符合硝酸钾溶解度变化规律的曲线。
查看答案和解析>>
科目: 来源: 题型:
右图为A、B两种固体物质的溶解度曲线。
(1)溶解度随着温度升高而增大的是 物质,t1℃时A、B两种物质的溶解度为 g.
(2)使一定量接近饱和的A物质溶液变成饱和溶液采用的一种方法是 。
(3)t1℃时,将一定量B的饱和溶液升温至t2℃,溶液的质量将 (填“增加”、“减少”或“不变”)。
 (4)t2℃时,分别用50gA、B制成饱和溶液,需要水的质量A B(填“>”“=”或“<”)。
(4)t2℃时,分别用50gA、B制成饱和溶液,需要水的质量A B(填“>”“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
实验室需配置一定浓度的硝酸钾溶液。
(1) 查阅硝酸钾溶解性。由右图可知,20℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配置40g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A、先移动游码到所需位置,再添加硝酸钾直到天平平衡
B、先添加所需的硝酸钾,再移动游码直到天平平衡
 (4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位1g/mL)
|
质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
查看答案和解析>>
科目: 来源: 题型:
右图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题
(1)碳酸钠和氯化钠混合溶液的pH____7(填“>”或“<”或“=”)
(2)40℃时,碳酸钠的溶解度为______g
(3)大于30℃时,碳酸钠的溶解度____氯化钠的溶解度(填“>”或“<”或“=”)
(4)40℃时,碳酸钠和氯化钠均饱和溶液,当温度降低到20℃时,析出的主要物质是______(填化学式)
(5)为检验(4)中析出的物质,取少量样品于试管中加入足量的______(填化学式)溶液,完全溶液,并有气体产生,再加入几滴稀______(填化学式)溶液,有白色沉淀产生。

查看答案和解析>>
科目: 来源: 题型:
《粗盐中难溶性杂质的去除》实验中,三次用到玻璃棒,其中第二次使用玻璃棒的作用是__________________,提纯后的食盐中还含有少量的CaCl2和MgCl2等可溶性杂质,将该食盐溶解后,依次加入过量的NaOH溶液,过量的_______(填化学式。下同)溶液,过滤,向滤液中加_____调节至pH=7,再将滤液蒸发结晶,即可得更纯的氯化钠。
查看答案和解析>>
科目: 来源: 题型:
遂宁市大英县境内的卓筒井是手工制盐的活化石,被誉为“中国古代第五大发明”、“世界石油钻井之父”,不仅是古代劳动人民勤劳、智慧的象征,也造福了千秋万代.其工艺流程包括下面五个步骤:

请结合所学化学知识,回答下列问题:
(1)第②步汲出的卤水浑浊,浓度一般在7~10度(即溶质质量分数为7%~10%,下同),这样的卤水咸度低,耗燃料,成本高,为了把卤水浓度提高18~20度,就产生了“晒卤”这一环节.在“晒卤”的过程中溶液溶质质量分数 (填“不变”、“变大”或“变小”).
(2)第④步“滤卤”和实验室“过滤”的原理一样,都是为了除去液体中的不溶性杂质.在实验室的过滤操作中,必须用到的玻璃仪器有:烧杯、玻璃棒、 ,其中玻璃棒的作用是 .
(3)第⑤步“煎盐”和实验室 结晶(填结晶的方法)的原理相同.
(4)如图是甲、乙、丙三种物质的溶解度曲线图,据图回答下列问题:
Ⅰ.甲、乙两种物质在 ℃时溶解度相同.
Ⅱ.t2℃时,甲、乙、丙三种物质溶解度由大到小排列为 .
Ⅲ.t4℃时,将三种物质各ag分别加入100g水中,充分溶解后,只有一种能形成饱和溶液,则a的取值范围是 .

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com