
科目: 来源: 题型:
犯罪分子常在黄金中混熔较多的铜,冒充纯金制品进行诈骗.小李要检验金制品中是否混有铜,他的检验步骤是:
(1)在酒精灯上灼烧金制品;
(2)将灼烧后的金制品在稀硫酸中浸一段时间.如果金制品中混有铜,应观察到的现象是 ;在稀硫酸中发生的化学 反应方程式是 ..
查看答案和解析>>
科目: 来源: 题型:
实验装置如图所示,在一个厚壁玻璃筒里放一块浸有少量乙醚(乙醚极易挥发)的棉花,用力把活塞迅速下压,棉花就会立即燃烧.根据该实验现象得出的下列结论正确的是( )

|
| A. | 气体比液体更容易被压缩 |
|
| B. | 浸有少量乙醚可以降低棉花的着火点 |
|
| C. | 活塞迅速下压,乙醚蒸气液化放出热量,使棉花燃烧 |
|
| D. | 外界对物体做功时,物体的内 |
查看答案和解析>>
科目: 来源: 题型:
下列关于溶液的说法正确的是( )
|
| A. | 某温度下两种不同物质的溶液,溶质质量分数相同,则这两种物质的溶解度一定相同 |
|
| B. | 溶质质量分数为10%的200毫升某溶液,密度为1.2克/厘米3,其中含溶质24克 |
|
| C. | 饱和溶液析出晶体后,溶质的质量分数一定减少 |
|
| D. | 不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大 |
查看答案和解析>>
科目: 来源: 题型:
某兴趣小组的同学,利用含有铁锈的铁粉制取四氧化三铁,在实验过程中还需要用到的仪器和药品合理的是( )

|
| A. | b(稀硝酸、锌粒)、c、d | B. | a(稀硫酸、锌粒)、c(高锰酸钾)、d、e |
|
| C. | a(双氧水、二氧化锰)、d | D. | c(氯酸钾、二氧化锰)、d(一氧化碳) |
查看答案和解析>>
科目: 来源: 题型:
2013年5月,质检部门在湖南某县生产的大米中检测出重金属镉含量超出国家标准,“镉大米”事件引起了广泛的关注.下列相关叙述错误的是( )
|
| A. | 导致大米镉含量超标的主要原因可能是当地土壤或水体中镉污染较严重 |
|
| B. | 大米中的镉可以通过食物链进入人体内,危害人体健康 |
|
| C. | 土壤中的镉可被水稻吸收并转运到通过无性生殖形成的种子中 |
|
| D. | 食用“镉大米”引起的中毒不是细菌性食物中毒 |
查看答案和解析>>
科目: 来源: 题型:
过度使用氮肥,是造成土壤和水体污染的一个重要原因.硝酸铵(NH4NO3)是一种常用的氮肥,其中氮元素的化合价是( )
|
| A. | ﹣3和+5 | B. | +2和+2 |
| ﹣5和+3 | D. | ﹣1和+5 |
查看答案和解析>>
科目: 来源: 题型:
过氧化氢溶液在存放过程中会自然分解,使溶质质量分数减小.某同学使用一瓶原标注为30%的过氧化氢溶液完成制取氧气的实验.通过称量,该瓶中共有116.8g溶液,取出13.6g在一定条件下进行实验,发现生成气体的质量与反应时间的关系如图所示.试计算
(1)现在这瓶过氧化氢溶液的溶质质量分数.
(2)该瓶溶液中,已经分解的过氧化氢质量.

查看答案和解析>>
科目: 来源: 题型:阅读理解
某学习小组对在实验中吸收过二氧化碳气体的碱石灰成分进行了研究.
【查阅资料】
①碱石灰是CaO与NaOH 的固体混合物,通常用于吸收二氧化碳及干燥气体.
②碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应.
【提出猜想】
该碱石灰的主要成分可能含有 、Ca(OH)2、CaCO3、NaOH和 .
【设计方案、收集证据】
(1)甲同学在烧杯中放入少量的碱石灰样品,加入足量蒸馏水充分搅拌,静置有白色沉淀,甲同学认为样品中一定含有CaCO3,乙同学认为他的结论不准确,原因是: N (填化学方程式).
(2)乙同学进一步设计实验并进行验证,过程如下:
| 实验操作 | 实验现象 | 实验结论 |
| ①从甲同学的烧杯中取少量上层清液于试管中,向其中滴加足量 溶液. | 有白色沉淀生成 | 生成白色沉淀的化学方程式为: . |
| ②过滤,向滤液中滴加无色酚酞试液. | 无明显现象 | 通过实验及分析,样品中不含有: . |
【解释与评价】
(1)乙同学进一步设计了下列实验装置,通过称量B装置的质量变化来确定样品的成分及质量(气密性良好,每步均完全反应,操作无误).
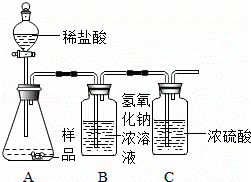
多次实验发现测定结果有时偏大有时偏小偏差,试分析其主要原因: .
(2)在老师的指导下乙同学完善了实验装置,并重新进行了实验,步骤如下: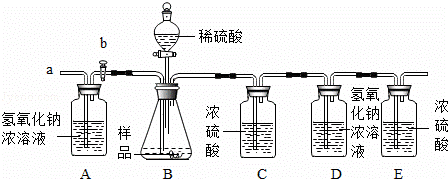
①检查装置气密性,将5.06g干燥的样品放入锥形瓶中;
②打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
③称量盛有氢氧化钠浓溶液的D瓶质量;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤打开活塞b,从导管a处缓缓鼓入一定量的空气;
⑥称量D瓶质量,增重2.2g.
通过分析及计算可知:5.06g样品中各成分及质量 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com