
科目: 来源: 题型:
实验室现有氯化镁和硫酸钠的固体混合物样品,小明同学想测定样品中氯化镁的质量分数。先称取该混合物样品20 g,完全溶于水中,然后取用了一定溶质质量分数的氢 氧化钠溶液100 g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
氧化钠溶液100 g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
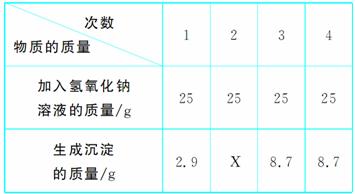
(1)上表中X的数值为________。
(2)计算原固体混合物样品中氯化镁的质量分数是多少?
(3)上述实验中所用到的氢氧化钠溶液,是小明同学利用实验室中已有的80 g溶质质量分数为30%的氢氧化钠溶液配制的,试计算需加入多少克水,才能配成实验中所需溶质质量分数的氢氧化钠溶液?
查看答案和解析>>
科目: 来源: 题型:
硝酸铵是农业生产中常用的化学肥料。为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取2.0 g该硝酸铵样品于容器中,滴入5.0 g 20%的NaOH溶液。发生如下反应:NH4NO3+NaOH===NaNO3+NH3↑+H2O。反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:

完成有关计算:
(1)NH4NO3中各元素的质量比为[m(H)∶m(N)∶m(O)]__________。
(2)样品中硝酸铵的质量分数。
(3)所得溶液中NaNO3的质量分数(保留两位小数)。
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组,在一次查阅“关于如何治疗人体胃酸过多”的资料后,决定利用实验室相关仪器(高温消毒)自制小苏打水(NaHCO3水溶液),用来缓解胃酸过多的症状。具体配制步骤(经医生建议)如下:
第一步:准确称量8.4 g食品级小苏打粉末;第二步:将第一步所称粉末配成100 g溶液;第三步:将第二步所得溶液取出10 g,再加水配制成100 g溶液即得到治疗胃酸过多的小苏打水(密度为1.0 g·mL-1)。
请回答下列问题:
(1)第一步用到的主要仪器是________;第二步使用的玻璃仪器有________(至少写两种)。
(2)第三步配制所得的小苏打水中NaHCO3的质量分数是________。
(3)胃酸过多者在医生的指导下,每次喝50 mL第三步配制所得的小苏打水,一天两次,则一天可反应掉胃液中的HCl________ g。
查看答案和解析>>
科目: 来源: 题型:
小煜通过学习知道:Na2CO3、NaHCO3均能与盐酸反应,Na2CO3溶液还会与石灰水反应。
【产生疑问】NaHCO3溶液也能与石灰水发生反应吗?如果能反应,生成物可能是什么?
【进行实验】小煜将NaHCO3溶液与石灰水混合,结果产生白色沉淀,已知Ca(HCO3)2能溶于水,碳酸氢盐在碱溶液中会生成碳酸盐。此白色沉淀是________________,证明NaHCO3溶液与Ca(OH)2溶液也能发生反应。为了进一步了解生成的含钠化合物有什么,继续探究:
【作 出猜想】①只有NaOH ②有Na2CO3和NaOH ③________
出猜想】①只有NaOH ②有Na2CO3和NaOH ③________
【实验设计】步骤1:取少量上述实验后的上层清液于试管中,再滴加足量的CaCl2溶液(中性),观察到产生白色沉淀,由此可知生成的含钠化合物一定含有________;
步骤2:将步骤1中反应后的混合物过滤,往滤液中先滴加几滴酚酞溶液,再滴加足量的稀盐酸,观察到溶液颜色变化情况为________,整个实验过程中无气泡产生,由此可知猜想②成立。
【拓展提高】若步骤1中未出现白色沉淀,则此时NaHCO3溶液与Ca(OH)2溶液反应的化学方程式为__________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
甲同学对有关盐的知识进行了以下的整理。
(1)填写下表空格中的化学式:
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| CaCl2 | NaCl | MgCl2 | AlCl3 |
反思:①根据以上盐中的金属元素的排列,可以得出是依据________顺序归纳整理的。
②酸在水溶液中能解离出H+,因此酸溶液具有相似的化学性质;碱在水溶液中能解离出OH-,因此碱溶液也具有相似的化学性质。请据此分析上述盐溶液是否会具有相似的化学性质?为什么?__________________________________________________________________。
(2)甲同学通过查阅资料,发现许多反应都有盐类物质生成。他将这些知识间的相互关系整理成下图。
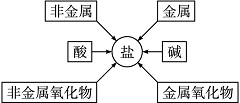
验证:请写出下列有盐生成的化学方程式:
①用稀硫酸除铁锈___________________________________________________________。
②盐酸与氢氧化钠反应______________________;属于________反应。
③古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,发生反应的化学方程式为__________________;属于________反应。
查看答案和解析>>
科目: 来源: 题型:
食醋、食盐和纯碱都是日常 生活中常用的物质。食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸,是一种无色液体。食盐和纯碱都是白色固体。
生活中常用的物质。食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸,是一种无色液体。食盐和纯碱都是白色固体。
(1)在用食醋拌凉菜时,往往可以闻到醋香,这说明醋酸具有________性。食醋不宜存放在含铁等金属的容器内,原因是______________________________。请写一个你熟悉的酸与金属反应的化学方程式____________________________。
(2)用食醋可以鉴别食盐和纯碱。请简要写出实验步骤和现象:___________________。
(3)纯碱的水溶液能使紫色石蕊溶液变蓝,说明其水溶液显________性,而在酸、碱、盐三类化合物中,纯碱属于________类。纯碱还能与许多化合物反应,请写一个你知道的纯碱与碱反应的化学方程式____________________________________。
查看答案和解析>>
科目: 来源: 题型:
某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2。小青同学设计了以下实验方案来除去可溶性杂质。
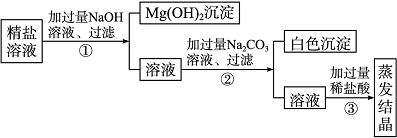
(1)步骤①的化学方程式为______________________________________________。
(2)步骤②中得到的白色沉淀是________(填化学式)。
(3)步骤③中加稀盐酸是为了除去溶 液中的________。
液中的________。
A.CaCl2 B.MgCl2
C.NaOH D.Na2CO3
查看答案和解析>>
科目: 来源: 题型:
小明家是种植蔬菜的专业户,他学习了九年级化学后告诉父母:施用适量的氮肥可以使种植的蔬菜叶色浓绿。因此:
(1)他建议父母去买的化肥是______。(填字母)
A.碳酸氢铵(NH4HCO3)
B.硫酸钾(K2SO4)
C.磷矿粉[Ca3(PO4)2]
(2) 他还告诉父母在施用氮肥的同时______(填“能”或“不能”)施用草木灰。理由是________________________________________________________________________。
他还告诉父母在施用氮肥的同时______(填“能”或“不能”)施用草木灰。理由是________________________________________________________________________。
(3)他还建议父母经常向大棚中补充气体肥料CO2,目的是促进绿色植物的________________ __作用。
__作用。
查看答案和解析>>
科目: 来源: 题型:
下列除去杂质的方法中,正确的是( )。
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaCl(Na2CO3) | 加入适量的Ca(OH)2 溶液、过滤 |
| B | CaO(CaCO3) | 加入水、过滤 |
| C | Cu(Fe) | 加入过量CuSO4溶液、过滤 |
| D | HNO3(H2SO4) | 加入适量Ba(NO3)2溶液、过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com