
科目: 来源: 题型:
小明同学将13.9 g含杂质的纯碱样品(碳酸钠与氯化钠的混合物)与90.5 g稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为______ g。
(2)请在下面的坐标图中,画出反应生成气体的质量(m)随时间(t)变化的曲线。

(3)求完全反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl===2NaCl+CO2↑+H2O)
查看答案和解析>>
科目: 来源: 题型:
物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙、丙三位同学按下面的步骤进行探究:
(1)提出假设:物质发生化学变化前后质量不变。
(2)设计并进行实验:甲设计的实验装置和选用药 品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。
品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。

写出A、B两个实验发生反应的化学方程式:________________,________________。
丙进行了图C所示的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平。然后,用酒精灯给a端铜丝加热数分钟。停止加热后冷却,他观察到的现象是________________________________________________________________________。
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙、丙认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
(4)你认为______的结论正确,请从原子的角度分析,结论正确的理由是________________________________________________________________________。
(5)导致其他实验结论错误的原因是______________________________。
查看答案和解析>>
科目: 来源: 题型:
图中A是高粱和薯类等经发酵、蒸馏得到的一种可再生能源,G为常见白色难溶盐。

(1)反应①的化学方程式是____________________。
(2)反应②的基本反应类型是____________。
(3)反应③的化学方程式是________________________。
查看答案和解析>>
科目: 来源: 题型:
写出下列反应的化学方程式:
(1)二氧化碳与水反应_______________________________________________________。
(2)电解水_________________________________________________________________。
(3)一氧化碳高温还原磁铁矿(主要成分Fe3O4)____________________________________
________________________________________________________________________。
(4)乙烯(C2H4)燃烧生成二氧化碳和水___________________________________________。
(5)向空中播撒碘化银(AgI)微粒可进行人工降雨,碘化银在光照条件下可分解为碘单质(I2)和银单质________________________________________________________________________
______________ __________________________________________________________。
__________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
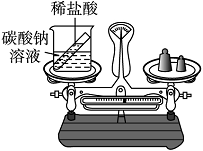
(1)在下图的装置中,当两种溶液发生反应后,天平不再保持平衡,指针向右偏转。天平不平衡的原因是__________________,反应的化学方程式为____________________。若反应物不变,要使天平在反应后仍然保持平衡,你认为对装置的改进措施是_____________。
(2)由质量守恒定律可知,化学反应前后,一定不变的是______(填序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目
⑤元素种类 ⑥物质种类
(3)硝酸在工业生产中有广泛的应用。工业上制取硝酸的关键反应为:4NH3+5O2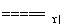 4NO+6R,其中R的化学式为______。
4NO+6R,其中R的化学式为______。
查看答案和解析>>
科目: 来源: 题型:
下面是某化学反应前后的微观模拟图,请根据图示回答:

(1)该化学反应中,参加反应的“ ”和“
”和“ ”与反应后生成的“
”与反应后生成的“ ”各粒子间的个数比为______。
”各粒子间的个数比为______。
(2)该反应的基本反应类型为______。
(3)根据上图所示,以具体物质为例,写出该反应的化学方程式________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
在化学反应2A+B2===2AB中,A与B2反应的质量关系如图所示,现将6 g A和8 g B2充分反应,则生成AB的质量是( )。
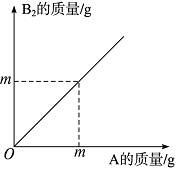
A.9 g B.11 g C.12 g D.14 g
查看答案和解析>>
科目: 来源: 题型:
下列化学反应方程式书写正确且有共同特点的是( )。
①Mg Cl2
Cl2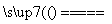 Mg+Cl2↑
Mg+Cl2↑
②2Fe+6HCl===2FeCl3+3H2↑
③3CO+Fe2O3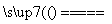 2Fe+3CO2
2Fe+3CO2
④NaCl+KNO3===KCl+NaNO3
⑤Ca(HCO3)2 CaCO3+CO2↑+H2O
CaCO3+CO2↑+H2O
⑥Na2CO3+BaCl2===BaCO3↓+2NaCl
A.①⑤ B.②③ C.④⑥ D.⑤⑥
查看答案和解析>>
科目: 来源: 题型:
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | m | 20 | 20 |
| 反应后质量/g | 2 | 待测 | 32 | 26 |
对该反应,下列描述正确的是( )。
A.该反应中甲、丙、丁的质量比为1∶16∶13
B.乙在该反应中一定是催化剂
C.待测质量一定为4 g
D.该反应是分解反应
查看答案和解析>>
科目: 来源: 题型:
化学实验中常常出现“1+1=2”或“1+1≠2”的有趣现象。下列符合“1+1=2”的事实是( )。
A.常温下,1 L水与1 L酒精混合后的体积等于2 L
B.室温下,1 g镁与1 g稀硫酸充分反应后所得的溶液质量为2 g
C.室温下,1 g硫粉在1 g氧气中完全燃烧后生成2 g二氧化硫
D.20 ℃,1 g氯化钠饱和溶液中加入1 g氯化钠固体能得到2 g氯化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com