
科目: 来源: 题型:
钙是维持人体正常功能所必需的元素。钙尔奇是常用的补钙剂,主要成分是CaCO3,钙尔奇每片2.0g。取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应)。烧杯内物质质量变为11.34g。试计算:
① 反应产生二氧化碳 (18) g,是 (19) mol;
② 每片钙尔奇中含碳酸钙 (20) mol;
③ 服用钙尔奇通常一日2次,每次1片。则每人每天摄入钙元素的质量为 (21) g。
④ 根据化学方程式列式计算上述反应所用稀盐酸溶质的质量分数(精确到0.01%)
(22)
查看答案和解析>>
科目: 来源: 题型:
利用下图装置可进行气体性质的探究实验。A处通入无色气体(可能是H2、CO或CO2);
B处玻璃管中盛放黑色粉末(可能是CuO或C),C处试管中盛放澄清石灰水。

① 根据要求完成下表填写:
| 序号 | 探究实验 | 简答 |
| Ⅰ | 若为H2与CuO的反应 | B处玻璃管观察到现象: (10) 。 |
| Ⅱ | 若为CO与CuO的反应 | B处反应的化学方程式: 发生氧化反应的物质是: (12) 。 |
| Ⅲ | 若为CO2与C 的反应 (B处换成酒精喷灯加热) | B处的黑色粉末逐渐减少,最后消失, D处观察到有 (13) 色的火焰。 |
② 探究实验Ⅰ通过B处的现象只能确定一种产物是铜,为了进一步确定另一产物是水,请对上述实验装置提出简要修改方案(添加或更换装置的位置和所需的药品) (14) 。
③ 探究实验Ⅱ澄清石灰水的作用(用发生反应的化学方程式表示) (15) 。
④ 在上述探究实验Ⅱ、Ⅲ中,D处导管尖嘴口都需用酒精灯点燃,简述其目的分别是:
(16) 、 (17) 。
查看答案和解析>>
科目: 来源: 题型:
小敏来到实验室完成氧气和二氧化碳气体的制取实验,请按照要求答问题:
① 实验台前有如下仪器和药品,请写出仪器A、B的名称:A (1) ,B (2) 。
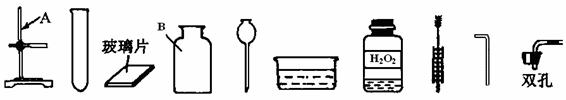
小敏利用上述仪器和药品可以做制取氧气的实验,实验前她发现其中缺少一种药品,
该药品名称是 (3) ;该反应的原理是(用化学方程式表示) (4) 。
② 下表是小敏实验时的主要步骤及相关实验装置,其中 (5) (填字母序号)步骤中的实验装置有错误,改正的方法是 (6) 。
改正后进行实验,这些步骤的正确操作顺序是 (7) (填字母序号)
| 实验 步骤 | a.制备气体 | b.收集气体 | c.检查装置气密性 | d.清洗仪器、整理桌面 |
| 相关 实验 装置 |
|
|
|
|
| ③ 利用上述装置另选药品,也能完成二氧化碳气体制备, 制取二氧化碳的化学方程式为 (8) 。 ④ 右图甲装置也可制取二氧化碳气体,甲装置的优点 是可随时控制反应的发生和停止。若打开弹簧夹, 固体与液体接触,反应便能发生,请简述使甲装置 中反应停止的原理 (9) 。 |
|
查看答案和解析>>
科目: 来源: 题型:
采用适当的试剂,可从石灰石(主要成分是CaCO3)中获得高纯度CaCO3,其流程如下:

① 流程图中进行的操作1、操作2的名称是 (26) ;
② 写出石灰石煅烧的化学方程式 (27) ,该反应的基本反应类型是 (28) 。
③ 该流程图所示物质中,溶于水放出大量热的氧化物是 (29) ,该物质与水反应的
化学方程式为 (30) 。
④ 使原料中各原子的利用率尽可能达到100%是“绿色化学”的核心理念之一。上述流程中有的物质可以再利用,该流程中可循环利用的物质是 (31) (填“化学式”)。
查看答案和解析>>
科目: 来源: 题型:
下表是KNO3 、NaCl在不同温度下的部分溶解度数据(单位:g/100g水),请回答问题:
① 10℃时,KNO3 溶解度是 (18) g/100g水。 ② 以上两种物质溶解度变化受温度影响较小的是 (19) 。 ③ 40℃时,将70gKNO3固体加入10 分搅拌,形成的溶液质量为 (20) g。 ④ 60℃时,KNO3的饱和溶液中含有少量NaCl, 通过 (21) 方法获得较纯净的KNO3晶体。 ⑤ 根据表中数据,请在坐标图中描点、绘制符合 KNO3溶解度变化规律的曲线 (22) 。 |
| ||||||||||||||||||
| ⑥ 向20mL水中溶解一定量KNO3固体的操作如右图: 请根据实验现象和溶解度数据回答:A、B、C中 溶液一定是饱和溶液的是 (23) ,一定是 不饱和溶液的是 (24) 。当x = (25) g 时,B中恰好没有固体剩余。 |
| ||||||||||||||||||
查看答案和解析>>
科目: 来源: 题型:
水是我们很熟悉的物质,通过化学学习之后,对水有了一些新的认识。
① 了解了水的宏 观组成,即水是由 (14) 元素组成的;
观组成,即水是由 (14) 元素组成的;
② 知道了水的微观结构,构成水的微粒是 (15) (填A、B、C、D字母序号);
A.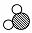 B.
B. C.
C.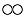
 D.
D.

③ 认识了用实验测定物质元素组成方法。化学家卡文迪什做的关于水的组成实验原理如下:
2H2+O2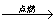 2H2O,请你从宏观角度描述该化学方程式表示的含义 (16) ;
2H2O,请你从宏观角度描述该化学方程式表示的含义 (16) ;
从微观角度,结合化学方程式,用②中微粒模型图示表示该化学反应的过程 (17)
|
| ||
| 反应物 | 生成物 |
查看答案和解析>>
科目: 来源: 题型:
碳是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关。
① 根据表中提供的信息,填写有关含碳物质的对应特性
| 物质用途 | 金刚石切割玻璃 | 石墨作电极 | 活性炭净水 |
| 对应特性 | 硬度大 | (6) | (7) |
 ② 金刚石、石墨和碳60都是由碳元素形成的单质,这些物质互称为碳元素的 (8) 。
② 金刚石、石墨和碳60都是由碳元素形成的单质,这些物质互称为碳元素的 (8) 。
③ CO2是宝贵的碳氧资源。CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为 (9) ,若要检验1%甲酸水溶液是否显酸性,能选用的有
(10) (填字母序号) a.无色酚酞溶液 b.紫色石蕊溶液 c.pH试纸
④ 化石燃料有煤、石油和天然气,它们都属于 (11) (填“可再生”或“不可再生”)能源。天然气最主要成分是甲烷,完全燃烧生成二氧化碳和水,该燃烧反应的化学方程式为 (12) 。从下表数据分析,与煤相比,用天然气作燃料的优点是 (13)。
| 1 g物质完全燃烧 | 甲烷 | 碳 |
| 产生二氧化碳的质量 / g | 2.75 | 3.67 |
| 放出的热量 / kJ | 56 | 32 |
查看答案和解析>>
科目: 来源: 题型:
现有氧气、氮气、氢气、一氧化碳、二氧化碳、二氧化硫、水、食盐等八种物质,
请按要求用化学式填写:
① 约占空气总体积4/5的是 (1) ; ② 最常用的溶剂是 (2) ;
③ 日常生活中用作调味料是 (3) ; ④ 导致酸雨的气体是 (4) ;
⑤ 能与血液里血红蛋白结合的有毒气体是 (5) 。
查看答案和解析>>
科目: 来源: 题型:
在CO、CO2混合气体中,氧元素的质量分数为64%。将该混合气体5g通过足量的灼热氧化铜,充分反应后,气体再全部通入足量的澄清石灰水中,得到白色沉淀的质量是
A.5g B.10g C.15g D.20g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com