
科目: 来源: 题型:
下列说法正确的是
A.同温同压下,H2 (g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H相同
B.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同
C.已知:①2H2(g) +O2(g) =2H2O(g) △H=-a kJ·mol-1,②2H2(g)+O2 (g)= 2H2O(1) △H=-b kJ·mol-1,则a>b
D.已知:①C(s,石墨)+O2 (g)=CO2(g) △H=- 393.5kJ·mol-1,②C(s,金刚石)+O2(g)=CO2 (g) △H=- 395.0 kJ·mol-1,则C(s,石墨)=C(s,金刚石) △H= -1.5 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,不正确的是
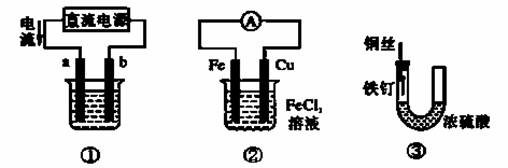
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.用装置①进行电镀,镀件接在b极上
C.装置②的总反应是:Cu+2Fe3+===Cu2++2Fe2+
D.装置③中的铁钉几乎没被腐蚀
查看答案和解析>>
科目: 来源: 题型:
500℃条件下,在恒容密闭容器中,充入1molNO2存在如下平衡2NO2(g) N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的
N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的
A.平衡向正反应方向移动 B.平衡常数K增大
C.NO2的转化率变小 D.容器内气体颜色先变深后变浅,最后比原来还要浅
查看答案和解析>>
科目: 来源: 题型:
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
A.溶液中导电粒子的数目增加,导电性增强 B.醋酸的电离程度增大,[H+]减小
C.再加入10mL pH=11 NaOH溶液,混合液pH=7 D.溶液中由水电离出的[H+]=1×10-11 mol/L
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.物质发生化学变化不一定伴随着能量变化
B.硫酸钡、醋酸铵、氨水都是弱电解质
C.用Na2S溶液与AlCl3溶液混合制取Al2S3
D.在温度、压强一定的条件下,自发反应总是向△H-T△S<0的方向进行
查看答案和解析>>
科目: 来源: 题型:
电池在生产、生活中应用越来越广泛。下列说法错误的是
A.化学电源有一次电池、可充电电池和燃料电池等,一次电池只能放电,不能充电
B.铅蓄电池应用广泛,主要优点是单位重量的电极材料释放的电能大
C.燃料电池具有能量利用率高、可连续使用和污染轻等优点
D.锂电池是一种高能电池,体积小、重量轻,单位质量能量比高
查看答案和解析>>
科目: 来源: 题型:
Ⅰ、下面是几种实验中常用的仪器:
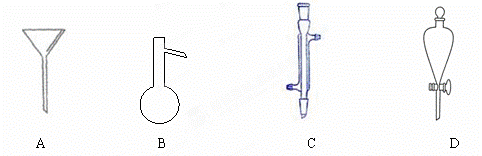
写出各序号所代表的仪器的名称:
A_____________;B_____________;C_____________;D_____________
Ⅱ、实验室需配制1.00mol/L的NaOH溶液100mL
(1)本实验用到的基本仪器已有烧杯、托盘天平(砝码、镊子)、玻璃棒、胶头滴管、量筒,还缺少的必要仪器是 。
(2)操作步骤的正确顺序为 (填序号)。
A、把制得的溶液小心地转移至容量瓶中。
B、在托盘天平上称取 g的NaOH固体,把它放在烧杯中,用适量的蒸馏水将它完全溶解并冷却至室温。
C、继续向容量瓶中加蒸馏水至液面距刻度l~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
D、取少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E、将容量瓶塞塞紧,充分摇匀。
(3)下列情况中,会使所配溶液浓度偏高的是 (填序号)。
A、某同学观察液面时俯视 B、没有进行上述的操作步骤D
C、加蒸馏水时,不慎超过了刻度线 D、选用的NaOH固体中混有Na2O
E、容量瓶使用前内壁沾有水珠
查看答案和解析>>
科目: 来源: 题型:
实验室常用下列装置来进行铜跟浓硫酸的反应实验。请回答下列问题:

(1)判断铜跟浓硫酸反应有SO2生成的依据是_____________________。
(2)装置乙的试管口放有一团浸有饱和氢氧化钠溶液的棉花,其目的是_______________,棉花中发生反应的离子方程式是__________________________________。
(3)实验中除了(1)小题中观察到的实验现象外,还可以观察到其它的实验现象,请你
任写一种: 。
(4) 实验室也可以利用上述装置进行木炭跟浓硫酸反应,写出碳跟浓硫酸反应的化学方程
式__________________________________。
查看答案和解析>>
科目: 来源: 题型:
单质A、B、C和化合物D、E、F,在一定条件下有如下图的转化关系:(有部分反应物或者生成物未标出)
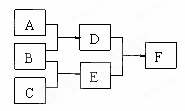
请回答下列问题:
(1)若A是空气中含量最多的气体,B在C中燃烧火焰呈苍白色。A与B反应生成D的化学方程式是__________________。D与E反应的现象是___________。D在催化剂作用下被氧气氧化是工业制备硝酸的主要反应之一,该反应的化学方程式是_____________。
(2)若A是金属单质,D是淡黄色固体,E在空气中含量增加会导致温室效应。则D的用途之一是__________,D与E反应生成F的化学方程式是__________________________。可以通过______________实验来检验D和F中所含的金属元素。
查看答案和解析>>
科目: 来源: 题型:
(1)实验室常用铜与浓硝酸反应来制取NO2气体,该反应的离子方程式是______
__________________________________。
(2)若将25.6g铜跟一定量的浓硝酸反应,铜耗完时,共产生11.2L气体(标准状况下),在该反应中,转移电子的数目是__________,则被还原的硝酸为________mol,生成NO2的体积为____________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com