
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:填空题
| 温度/℃ | 25 | 150 | 300 | 350 | 400 | 450 | 500 | 600 | 700 | 800 |
| 固体质量/g | 2.000 | 1.804 | 1.600 | 1.600 | 0.800 | 0.800 | 0.888 | 0.888 | 0.860 | 0.860 |
查看答案和解析>>
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:解答题
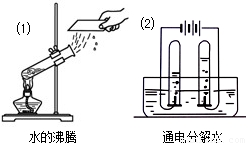
查看答案和解析>>
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:解答题
 某市环保部门绘制的四年来该地区全年降雨的平均pH变化示意图,请回答下列问题:
某市环保部门绘制的四年来该地区全年降雨的平均pH变化示意图,请回答下列问题:查看答案和解析>>
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:解答题

查看答案和解析>>
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:解答题
| 序号 | 配制100g10%的KOH的溶液的方案设计 |
| 方案1 | |
| 方案2 |
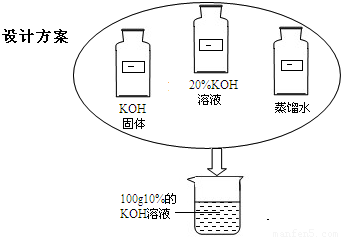
查看答案和解析>>
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:解答题
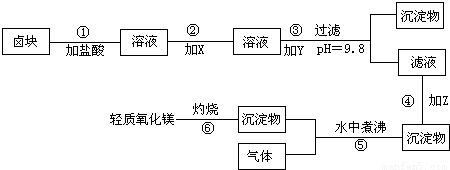
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 工业品 | 规格 | 价格(元.╱吨) |
| 漂液 | 含NaClO 25.2% | 450 |
| 过氧化氢 | 含H2O230% | 240 |
| 烧碱 | 含NaOH 98.5% | 2100 |
| 纯碱 | 含Na2CO399.5% | 600 |
| 卤块 | 含MgCl2 30% | 310 |
查看答案和解析>>
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:解答题
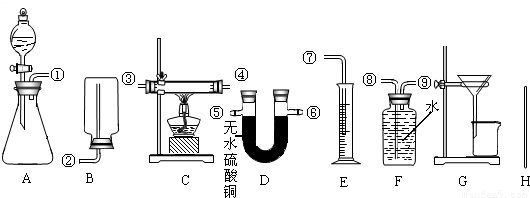
| 选用药品的名称(1) | 选用的实验装置及组装时接口的连接顺序(2) | 需测得的实验数据(从上述可测得的数据中选取)(3) | 合金中锌的质量分数的计算式(4) | ||
| 选用的实验装置序号 | 组装时接口编号的连接顺序(如不需要组装,则不填) | ||||
| 方案一 | |||||
| 方案二 | |||||
| 方案三 | |||||
查看答案和解析>>
科目: 来源:2005年第十五届“天原杯”全国初中学生化学素质和实验能力竞赛(湖南赛区)初赛试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2008年第十八届“天原杯”全国初中学生化学素质和实验能力竞赛(山西赛区)初赛试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2008年第十八届“天原杯”全国初中学生化学素质和实验能力竞赛(山西赛区)初赛试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com