
科目: 来源: 题型:单选题
| 废液来源 | 甲组 | 乙组 |
| 检测方法与结果 | 观察废液呈无色 | 观察废液呈红色 |
查看答案和解析>>
科目: 来源: 题型:填空题
 氢氧化钠溶液与稀硫酸反应的化学方程式为________.实验室有一瓶标签残缺的硫酸溶液,为了粗略测定每毫升硫酸溶液中溶质H2SO4的物质的量(单位:mol/mL),其实验步骤如下:
氢氧化钠溶液与稀硫酸反应的化学方程式为________.实验室有一瓶标签残缺的硫酸溶液,为了粗略测定每毫升硫酸溶液中溶质H2SO4的物质的量(单位:mol/mL),其实验步骤如下:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
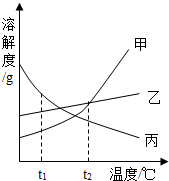
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
 人的胃液里含有适量的盐酸,可帮助消化,但如果分泌过多,人会感到胃痛.小军拿来了一种治疗胃酸过多的药物,该药物说明书的部分内容如图所示.
人的胃液里含有适量的盐酸,可帮助消化,但如果分泌过多,人会感到胃痛.小军拿来了一种治疗胃酸过多的药物,该药物说明书的部分内容如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com