

科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
| 事实 | 解释 | |
| A | 二氧化碳气体经降温、加压变成干冰 | 分子之间有间隔 |
| B | 炎热的夏天自行车胎容易爆裂 | 分子运动加快 |
| C | 水电解产生氢气和氧气 | 分子是可以再分的 |
| D | 倒有开水的热水瓶的瓶口有白雾 | 水分子能保持水的化学性质 |
查看答案和解析>>
科目: 来源: 题型:解答题
 铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.
铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.| 配置用水 | 有浑浊 | 有浑浊 |
| 自来水 | 无浑浊 | 有浑浊 |
| 市售纯净水 | 无浑浊 | 有浑浊 |
| 医用纯净水 | 无浑浊 | 无浑浊 |
| 试验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 饱和溶液 | 2 | 4 | 6 | 8 | 16 | 32 | 128 |
| 现 象 | 白色浑浊→澄清 | ||||||
查看答案和解析>>
科目: 来源: 题型:解答题
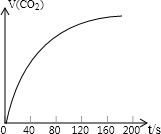
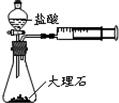 某实验小组利用下图装置对实验室制取CO2的速率快慢进行了研究.他们实验时所用的试剂和使用的反应条件如下表所示:
某实验小组利用下图装置对实验室制取CO2的速率快慢进行了研究.他们实验时所用的试剂和使用的反应条件如下表所示:| 盐酸 | 大理石 | 温度条件 |
| 5% | 细颗粒 | 20℃ |
| 10% | 粗颗粒 | 40℃ |
| 每次用量均 | 每次用量均5g |
| 实验编号 | 温度 | 大理石规格 | HCl浓度 | 探究目的 |
| ① | 20℃ | 粗颗粒 | 5% | (I)实验①和②探究浓度对反应快慢的影响; (II)实验②和________探究温度对反应快慢的影响; (III)实验________和________探究大理石粗、细对反应快慢的影响. |
| ② | 20℃ | 粗颗粒 | ________ | |
| ③ | ________ | 细颗粒 | 5% | |
| ④ | 40℃ | ________ | 10% |
查看答案和解析>>
科目: 来源: 题型:多选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com