
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:选择题
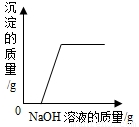
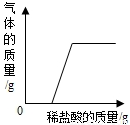
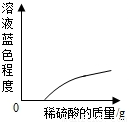
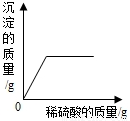
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:填空题
 今年为增强内需促进经济发展,家用汽车发展较快.
今年为增强内需促进经济发展,家用汽车发展较快.查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:填空题
| 20℃ | NaCl | NaOH | NH4NO3 |
| 溶解度(g) | 36 | 109 | 192 |
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:解答题
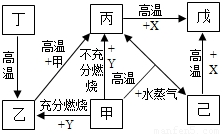
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:解答题
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| CaCl2 | NaCl | MgCl2 | AlCl3 |

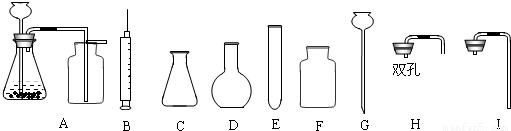
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:解答题
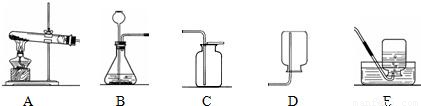
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:解答题
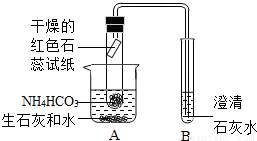
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:解答题
| 实验步骤及操作方法 | 实验现象 | 结 论 |
| 假设③成立 |
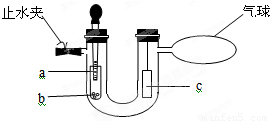
查看答案和解析>>
科目: 来源:2011年江苏省扬州一中中考化学模拟试卷(解析版) 题型:解答题
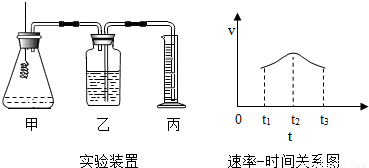
| 实验步骤 | 实验现象 | 实验结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com