
科目: 来源:2007年江苏省扬州市中考化学试卷(解析版) 题型:填空题
| 专题2:物质性质和用途 No:WZ09 摘录时间2011年3月20日 工业用盐 致癌作用 含+3价氮 该物质式为________ 制取氧气 暗紫色固体 可用于消毒盐 该物质式为________ 无色无味 剧毒气体 与血红蛋白结合 该物质式为________ 一种氮肥 含氮 35% 溶于水温度下降 该物质式为________ |
查看答案和解析>>
科目: 来源:2007年江苏省扬州市中考化学试卷(解析版) 题型:填空题
查看答案和解析>>
科目: 来源:2007年江苏省扬州市中考化学试卷(解析版) 题型:填空题


查看答案和解析>>
科目: 来源:2007年江苏省扬州市中考化学试卷(解析版) 题型:解答题

查看答案和解析>>
科目: 来源:2007年江苏省扬州市中考化学试卷(解析版) 题型:解答题
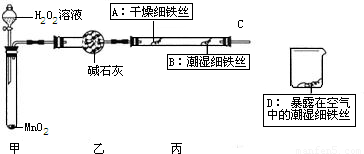
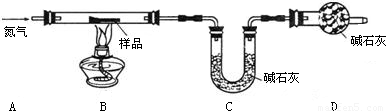
查看答案和解析>>
科目: 来源:2011年黑龙江省哈尔滨市中考化学试卷(解析版) 题型:选择题
 (2011?哈尔滨)2011年6月10日,作为哈尔滨市“中兴”重点建设项目的宣化街高架桥工程,历经205个日夜的建设正式竣工通车,这使冰城交通路网格局将更加畅通.下列叙述错误的是( )
(2011?哈尔滨)2011年6月10日,作为哈尔滨市“中兴”重点建设项目的宣化街高架桥工程,历经205个日夜的建设正式竣工通车,这使冰城交通路网格局将更加畅通.下列叙述错误的是( )查看答案和解析>>
科目: 来源:2011年黑龙江省哈尔滨市中考化学试卷(解析版) 题型:选择题
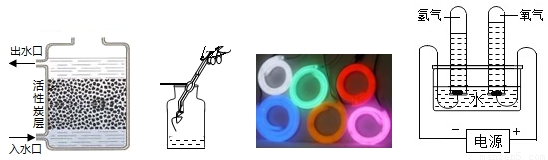
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com